工业制硫酸中的反应:2SO2+O2 2SO3,等量的反应物在两个容器中反应,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若平衡时甲容器中SO2的百分含量p%,则平衡时乙容器中SO2的百分含量
2SO3,等量的反应物在两个容器中反应,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若平衡时甲容器中SO2的百分含量p%,则平衡时乙容器中SO2的百分含量
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
100 mL 6 mol·L-1的H2SO4溶液跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
①Na2CO3溶液 ②水 ③K2SO4溶液 ④KNO3溶液
| A.①③ | B.②③ | C.①④ | D.②④ |
现有乙酸、乙烯和丙烯(C3H6)的混合物,其中氧的质量分数为a,则碳的质量分数是()
A. |
B.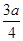 |
C.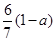 |
D.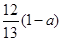 |
某有机物的结构如图,这种有机物不可能具有的性质是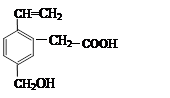
| A.能使Br2的四氯化碳溶液褪色 |
| B.能发生酯化反应 |
| C.能发生水解反应 |
| D.能跟Na反应 |
下列实验方案不合理的是( )
| A.除去乙烷中含有的乙烯:将气体通入溴水中,洗气 |
| B.检验蔗糖是否水解:取1mL 20%的蔗糖溶液,加3~5滴稀硫酸。水浴加热5min后取少量溶液,加氢氧化钠溶液调溶液pH至碱性,再加入少量新制备的Cu(OH)2,加热3~5 min,观察实验现象 |
| C.除去乙酸乙酯中的乙酸:加入浓硫酸和乙醇,加热 |
| D.鉴别己烯和苯:将溴的四氯化碳溶液分别滴加到少量己烯和苯中 |
反应3X(g)+Y(g) 2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的平均速率υ为( )
2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的平均速率υ为( )
| A.υ(X)=0.05mol·L—1·min—1 | B.υ(Y)= 0.10mol·L—1·min—1 |
| C.υ(Z)=0.10mol·L—1·min—1 | D.υ(W)=0.05mol·L—1·s—1 |