今已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3 +6HCl=3Cl2+KCl +3H2O,
③2KBrO3 +Cl2=Br2 + 2KClO3,下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.反应②中还原剂与氧化剂的物质的量之比为6∶1 |
| C.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
| D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
下图是可逆反应A+2B  2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断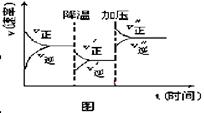
A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.D可能是气体.
D.A、B、C、D均为气体
已知25℃、101kPa条件下:
①4Al(s)+3O2(g)=2Al2O3(s);△H=-2834.9kJ•mol-1
②4Al(s)+2O3(g)=2Al2O3(s);△H=-3119.1kJ•mol-1由此得出的正确结论是
| A.等质量的O2比O3能量低,由O2变O3为吸热反应 |
| B.反应①可确定铝的燃烧热是708.7KJ |
| C.O3比O2稳定,由O2变O3为放热反应 |
| D.反应②可确定铝的燃烧热是779.78 kJ•mol-1 |
已知中和热的数值是57.3KJ/mol。下列反应物混合时,产生的热量等于57.3KJ 的是
| A.500mL1 mol/LHCl(aq)和500mL 1mol/LNaOH(aq) |
| B.500mL 1mol/LH2SO4(aq)和500mL 1mol/LBa(OH)2(aq) |
| C.1000mL1.0mol/L的CH3COOH(aq)和1000mL1.0mol/L的NaOH(aq) |
| D.1000mL1.0mol/L的HCl(aq)和1000mL1.0mol/L的NaOH(aq) |
、某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)  Z(g)+W(s);ΔH>0下列叙述正确的是
Z(g)+W(s);ΔH>0下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.当容器中气体压强不变时,反应达到平衡状态 |
| C.升高温度,平衡逆向移动 |
| D.平衡后加入X,上述反应的ΔH增大 |
在一定温度下,向密闭容器中充入1.0molN2和3.0molH2,反应在一定压强下,达到平衡时测得NH3的物质的量为0.6mol。若在该容器中开始时充入2.0 molN2和6.0molH2,则平衡时NH3的物质的量为
| A.若为定容容器,n(NH3)=1.2mol | B.若为定压容器,n(NH3) >1.2mol |
| C.若为定容容器,n(NH3)>1.2mol | D.若为定压容器,n(NH3)<1.2mol |