某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察_________
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是___________________________
(5)如图,是某次滴定时的滴定管中的液面,其读数为 mL

(6)
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前度数(mL) |
滴定后度数(mL) |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
4.00 |
24.10 |
请计算待测烧碱溶液的浓度 mol/L.
锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验窒重要的分析试剂,工业上常用天青石(主要成分为SrSO4)为原料制备,生成流程如下:
已知:①经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
②SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③SrCl2•6H2O的摩尔质量为:267g/mol.
(1)天青石焙烧前先研磨粉碎,其目的是_________________
(2)隔绝空气高温焙烧,若0.5mol SrSO4中只有S被还原,转移了4mol电子.写出该反应的化学方程式_________________
(3)为了得到较纯的六水氯化锶晶体,过滤2后还需进行的两步操作是_________________
(4)加入硫酸的目的是_________________;为了提高原料的利用率,滤液中Sr2+的浓度应不高于__________ mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。
(5)产品纯度检测:称取1.000g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2mol的AgNO3溶液(溶液中除Cl-外,不含其它与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。①滴定反应达到终点的现象是_________________;
②若滴定过程用去上述浓度的NH4SCN溶液20.00mL,则产品中SrCl2•6H2O的质量百分含量为_______(保留4位有效数字)。
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。
CO(NH2)+2NaOH+NaClO═Na2CO3+N2H4•H2O+NaCl
NaClO过量时,易发生N2H4•H2O+2NaClO═N2↑+2NaCl+3H2O
实验一:制备NaClO溶液.(实验装置如图1所示)
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有______________(填标号);
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的化学方程式是______________;
实验二:制取水合肼.(实验装置如图2所示)
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应.加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(已知:N2H4•H2O+2NaClO═N2↑+3H2O+2NaCl)
(3)分液漏斗中的溶液是_______(填标号);
A.CO(NH2)2溶液
B.NaOH和NaClO混合溶液
选择的理由是______________;
实验三:测定馏分中肼含量
称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL,用0.1000mol•L-1的I2溶液滴定.滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4•H2O+2I2═N2↑+4HI+H2O)
(4)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,用离子方程式解释其原因______________;
(5)实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4•H2O)的质量分数为___________;
高纯度氧化铝有广泛的用途,某研究小组用以下流程制取高纯度氧化铝: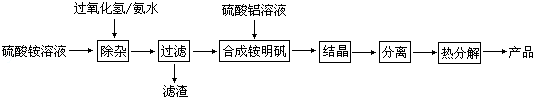
根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+.请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式
(2)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是
(3)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水).母液不能蒸干的原因是 .
(4)“分离”操作的名称是 (填字母代号).
A.蒸馏 B.分液 C.过滤
(5)铵明矾晶体的化学式为NH4Al(SO4)2•12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是 ,离子浓度最小的离子是 .
一定量的浓硫酸与足量Zn充分反应时,有SO2和H2生成。某校化学研究性学习小组对此进行研究。按图组装好实验装置,微热试管A,观察到C、D、E中均有气泡产生;随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失;反应较长时间后,C、D、E中的气泡量又会明显增加。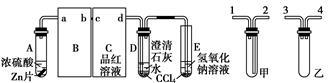
请回答:
(1)装置A中需用浓H2SO4,用一种简单的方法确定一瓶H2SO4一定是浓H2SO4:__________________。
(2)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接________、________接b,c接 ________、________接d;D、E两支试管中CCl4的作用是_____________________。
(3)能证明浓硫酸具有强氧化性的实验现象为____________________________;
反应较长时间后气泡量又会明显增加的原因是__________________________________。
(4)D中浑浊消失的离子反应方程式为________________________________。
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应),某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定;
①按如图组装仪器,检查装置的气密性;
②将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品都为碱石灰(详见图示,夹持仪器省略)
③从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却.
(1)装置C的作用为__________________;
(2)测的反应后装置B增重1.35g,则铁矿石中氧的百分含量为__________________;
(3)若将H2换成CO,则还需补充___________装置。
Ⅱ.铁矿石中含铁量的测定
(1)步骤④中煮沸的作用是__________________;
(2)步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、__________________;
(3)下列有关步骤⑥的操作中说法正确的是__________
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测液润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色再读数
(4)若滴定过程中消耗0.5000mol•L-1KI溶液20.00ml,则铁矿石中铁的百分含量为________________;
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为_______________。