在一密闭容器中发生反应N2+3H2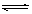 2NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
2NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
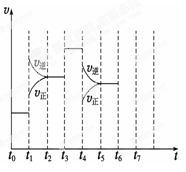
(1)处于平衡状态的时间段是 (填选项)。
A.t0~t1
B.t1~t2
C.t2~t3
D.t3~t4
E.t4~t5
F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是_____(填选项)。
A.增大压强
B.减小压强
C.升高温度
D.降低温度
E.加催化剂
F.充入氮气
t1时刻 ;t3时刻 ;t4时刻 。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是 (填选项)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线。
(5)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为 。
以下是对重要非金属及其化合物的讨论,根据要求回答问题:
(1)实验室盛装NaOH溶液是试剂瓶不能用玻璃塞,应该用橡胶塞,以防止发生反应:
(离子方程式)。
(2)氨是一种重要的化工产品,密度比空气 (填“大”或“小”)。工业上制备氨气的化学方程式为。
(3)工业上制取漂白粉的反应化学方程式为。
(4)浓H2SO4常用作气体干燥剂,是因为它具有____________;将适量的蔗糖放入烧杯中,滴入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。请回答:
产生刺激性气味气体的化学方程式为。
(5)铜和稀硝酸反应的离子方程式是。若参加反应的Cu质量为6.4g,生成NO气体____________L(标准状况下),则转移电子物质的量为mol,被还原的与未被还原的HNO3物质的量之比为。
以下是对金属及其化合物的讨论,根据要求回答问题
(1)写出钠与水反应的离子方程式。
(2)在AlCl3溶液中逐滴滴入过量的NaOH溶液,观察到的现象是,
反应的离子方程式为,。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为。
(1)常温下pH="5" HCl溶液和pH=5的AlCl3溶液中由水电离产生的c (H+) 之比等于。
(2)写出泡沫灭火器灭火时发生反应的离子方程式。
(3)常温下将0.01molCH3COONa和0.02mol盐酸溶于水,配成0.5L混合溶液。溶液中共有种微粒,各离子浓度从大到小的顺序为。
(4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(忽略溶液混合时的体积变化)。
回答下列问题:
①由图中信息可知HA为_______酸(填“强”或“弱”) ② K点对应的溶液中c(M+)+c(MOH)=mol·L-1。
固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO来生产甲醇燃料的方法: CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H = -49.0 kJ·mol-1,
CH3OH(g)+H2O(g)△H = -49.0 kJ·mol-1,
某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。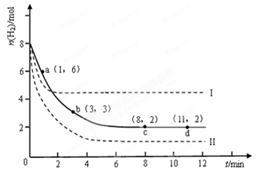
(1)a点正反应速率_______(填大于、等于或小于)逆反应速率。
(2)下列时间段平均反应速率最大的是__________。
| A.0~1min | B.1~3min | C.3~8min | D.8~11min |
(3)求平衡时CO2的转化率和该条件下的平衡常数K。
(4)仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是,曲线II对应的实验条件改变是。
为探究某抗酸药X的组成,进行如下实验:
查阅资料:
①抗酸药X可能的组成可以表示为:MgmAln(OH)p(CO3)q(SiO3)r(m、n、p、q、r为≥0的整数)。
② 在pH=5.0时沉淀完全;
在pH=5.0时沉淀完全; 在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
实验过程:
| 步骤 |
实验操作 |
实验现象 |
| I |
向X的粉末中加入过量盐酸 |
产生气体A,得到无色溶液 |
| II |
向Ⅰ所得的溶液中滴加氨水,调节pH至5~ 6,过滤 |
生成白色沉淀B |
| III |
向沉淀B中加过量NaOH溶液 |
沉淀全部溶解 |
| IV |
向II得到的滤液中滴加NaOH溶液,调节pH至12 |
生成白色沉淀C |
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是。
(2)II中生成B反应的离子方程式是。
(3)III中B溶解反应的离子方程式是。
(4)沉淀C的化学式是。
(5)若上述n(A)︰n(B)︰n(C)=1︰2︰3,则X的化学式是。