利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。则下列说法不正确的是 ( )
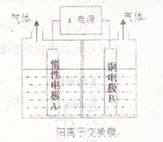
| A.外加电源的a极为正极 |
| B.电解过程中,Li+向B极迁移 |
| C.阳极反应式为:4OH--4e-=O2↑+H2O |
| D.每生成1molLiOH,外电路转移1mol电子 |
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)===CO2(g) ΔH1 C(s)+1/2O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+1/2O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)===Ca(OH)2(s) ΔH8
| A.① | B.④ | C.②③④ | D.①②③ |
将一定量的Ag2SO4固体置于容积不变的容器中,在某温度下发生下列反应:
Ag2SO4(s)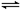 Ag2O(s)+SO3(g),2SO3(g)
Ag2O(s)+SO3(g),2SO3(g)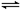 2SO2(g)+O2(g),经十分钟后,反应达到平衡,此时C(SO3)=0.4 mol/L,C(SO2)=0.1 mol/L,则下列叙述不正确的是
2SO2(g)+O2(g),经十分钟后,反应达到平衡,此时C(SO3)=0.4 mol/L,C(SO2)=0.1 mol/L,则下列叙述不正确的是
| A.SO3的分解率为20% | B.平衡时,v(O2)=0.005 mol/(L·min) |
| C.容器内气体的密度为40g/L | D.加压,容器内固体质量不变 |
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加入3molZ,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):aX(?)+2Y(?) 3Z(g)。此时Ⅱ中X、Y、Z的物质的量之比为1:2:2,则下列说法一定正确的是
3Z(g)。此时Ⅱ中X、Y、Z的物质的量之比为1:2:2,则下列说法一定正确的是
| A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| B.若X、Y不均为气态,到达平衡后若在Ⅰ中再加入1molZ,则新平衡时Y的体积分数变大 |
| C.若X、Y均为气态,则从起始到平衡所需时间:Ⅰ>Ⅱ |
| D.若X、Y不均为气态,到平衡后若在Ⅱ中再加入2molZ,则新平衡时Z的体积分数变小 |
在某一密闭容器中,充入一定量的HI气体,发生反应2HI(g) H2(g)+I2(g),(正反应吸热)。在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是
H2(g)+I2(g),(正反应吸热)。在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是
将a g光亮的铜丝在酒精灯上加热后,迅速插入下列溶液中,然后取出干燥,如此反复几次,最后取出铜丝,洗涤、干燥后称其质量为b g。下列所插入的物质与铜丝质量关系不正确的是( )
| A.无水乙醇:a=b | B.石灰水:a>b |
| C.NaHSO4溶液:a>b | D.盐酸:a>b |