对于物质的量浓度均为0.01 mol/L的①NaHCO3、②Na2CO3、③CH3COOH、④CH3COONa四种溶液,下列说法正确的是
| A.①的离子浓度为:c(Na+)>c(OH-)>c(HCO3-)>c(H+) |
| B.②c(OH﹣)=c(HCO3﹣)+c(H+)+c(H2CO3) |
| C.③加入等体积的水稀释,电离平衡正向移动,c(H+)增大 |
| D.④和③等体积混合,c(CH3COO-)+c(CH3COOH)="0.01" mol/L |
下列实验不能达到目的的是
| A.用溴水除去CH4中混有的C2H4 |
| B.用加热蒸干Na2CO3溶液的方法制备无水Na2CO3固体 |
| C.用分液漏斗分离苯萃取碘水后已分层的有机层和水层 |
| D.加热除去NH4Cl中的少量NaHCO3 |
下列说法不正确的是
| A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂 |
| B.SiO2有导电性,可用于制备光导纤维 |
| C.硅胶常用作实验室和食品、药品等的干燥剂,也可作催化剂载体 |
| D.小苏打是一种膨松剂,可用于制作馒头和面包 |
下列离子方程式书写正确的是
| A.将少量的H2S气体通入硫酸铜溶液中: H2S+Cu2+=CuS↓+2H+ |
| B.将NO2气体通入水中:2NO2+H2O= NO3-+ NO↑+2H+ |
| C.ICl 和Cl2的化学性质相似,将ICl通入KOH溶液中:ICl+2OH-=I-+ ClO-+H2O |
| D.往100ml 1.5mol/L的FeBr2溶液中通入0.15mol Cl2:2Br-+Cl2=Br2+2Cl- |
短周期元素R、T、Q、W在元素周期表中的相对位置如下图所示,其中 T 所处的周期序数与族序数相等。下列判断不正确的是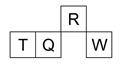
| A.最简单气态氢化物的热稳定性:R > Q |
| B.最高价氧化物对应水化物的酸性:Q < W |
| C.原子半径:T > Q > R |
| D.含T的盐溶液一定显酸性 |
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
| A.该反应的△H>0 |
| B.其他条件不变,升高温度反应的平衡常数增大 |
C.300℃时,0-t1min内 CH3OH的平均生成速率为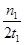 mol·L-1 min-1 mol·L-1 min-1 |
| D.A点的反应体系从300℃升高到500℃,达到平 |
衡时 减小
减小