填空题。
(1)用以下五种物质的编号进行填空:①甲烷 ②苯 ③乙醇 ④蚁酸 ⑤淀粉 其中:
能发生银镜反应的是 ;燃烧时产生浓烟的是 ;分子结构是正四面体的是 ;
遇碘水显蓝色的是 ;工业上可用乙烯水化法制备得到的是 。
(2)按要求填空:
①葡萄糖的分子式 ; ②乙炔的电子式 ; ③2-甲基-1-戊烯的键线式 。
(3)写出下列反应的化学方程式:
①溴乙烷在氢氧化钠的醇溶液中共热 。
②乙酸乙酯在氢氧化钠的水溶液中共热 。
化合物A、B、C、D、E分别由H+、Na+、Al3+、Cu2+四种阳离子和CO32-、Br-、SiO32-、SO42-四种阴离子组成。已知①A、B、C三种溶液pH<7,D、E溶液pH>7②A、C的阴离子相同,D、E的阳离子相同③用石墨电极电解A的溶液,阳极有无色气体产生,阴极有红色物质生成④C溶液与D溶液反应能生成一种白色沉淀和一种气体,且此沉淀可溶于B的溶液,此气体通入E的溶液中可产生另一种白色沉淀。
请根据以上事实填空:
⑴写出B、C、E的化学式:B___________、C___________、E____________。
⑵D溶液的pH>7,原因是:(结合离子方程式说明)__________________________________。
⑶写出C溶液与D溶液发生反应的离子方程式:_______________________。
⑷若用石墨电极电解400mL 1.0 mo1·L—1 A的溶液,当阳极有2.24 L气体(标准状况)产生时,溶液的pH=_______________(设溶液的体积不变)。
(8分)在一定条件下可实现下图所示物质之间的变化: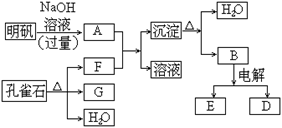
请填写以下空白:
(1)孔雀石的主要成分是Cu2(OH)2CO3,受热易分解。上图中的F的电子式为。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式。
(3)图中所得G和D都为固体,混和后在高温下可发生反应,写出该反应的化学方程式。
(4)D与NaOH溶液反应的化学方程式为(用单线桥标出电子转移的方向及数目)。
(9分)芳香族化合物C的分子式为C9H9OCl。C分子中有一个甲基且苯环上只有一条侧链;一定条件下C能发生银镜反应;C与其他物质之间的转化如下图所示: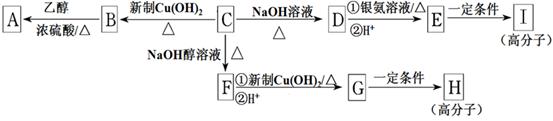
(1)F中含氧官能团的名称是;B→A的反应类型是。
(2)C的结构简式是,H的结构简式是。
(3)写出下列化学方程式:
① D与银氨溶液反应___________;② E→I。
(4)有的同学认为B中可能没有氯原子,你是__________(填“同意”或“不同意”),你的理由_______________。
(5)D的一种同系物W(分子式为C8H8O2)有多种同分异构体,则符合以下条件W的同分异构体有________种,写出其中核磁共振氢谱有4个峰的结构简式____________。
①属于芳香族化合物
②遇FeCl3溶液不变紫色
③能与NaOH溶液发生反应但不属于水解反应
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4 ( g ) + H2O ( g )=CO ( g ) + 3H2 ( g )△H =+206.0 kJ·mol-1
II:CO ( g ) + 2H2 ( g )=CH3OH ( g )△H=—129.0 kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的热化学方程式为。
(2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为100 L的反应室,在一定条件下发生反应I,测得在一定的压强下CH4的转化率与温度的关系如右图。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为。
②100℃时反应I的平衡常数为。
(3)在压强为0.1 MPa、温度为300℃条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下发生反应II生成甲醇,平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是(填字母序号)。
| A.c ( H2 )减少 | B.正反应速率加快,逆反应速率减慢 |
| C.CH3OH 的物质的量增加 | D.重新平衡c ( H2 )/ c (CH3OH )减小 |
E.平衡常数K增大
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用右图装置模拟上述过程: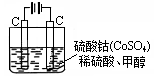
①写出阳极电极反应式。
②写出除去甲醇的离子方程式。
③若右图装置中的电源为甲醇—空气—KOH溶液的燃料电池,则电池负极的电极反应式:,净化含1 mol甲醇的水燃料电池需消耗KOH
mol。
(9分)已知X、Y、Z是阳离子,K是阴离子,M、N是分子。它们都由短周期元素组成,且具有以下结构特征和性质:
①它们的核外电子总数都相同;
②N溶于M中,滴入酚酞,溶液变红;
③Y和K都由A.B两元素组成,Y核内质子数比K多2个;
④X和N都由A、C两元素组成,X和Y核内质子总数相等;
⑤X和K的浓溶液在加热条件下生成M和N;
⑥Z为单核离子,向含有Z的溶液中加入少量含K的溶液,有白色沉淀生成,再加入过量的含K或Y的溶液,沉淀消失。
回答下列问题:
(1)Y的化学式为;N的电子式为
(2)试比较M和N的稳定性:M(填“>”或“<”)N。
(3)写出Z和N的水溶液反应的离子方程式:;
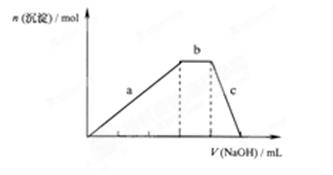
(4))上述六种微粒中的两种可与硫酸根形成一种含三种离子的盐,向该盐的浓溶液中逐滴加入0.1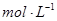 的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
的NaOH溶液,出现了如图中a、b、c三个阶段的图像,
①写b出阶段的离子方程式:
②根据图像判断该盐的化学式为。