《化学与生活》
(1)下列常用物质: A 碳酸氢钠 B 阿斯匹林 C 葡萄糖 D 苯甲酸钠 E 柠檬黄
请用字母填空:
具有解热镇痛疗效的是 ,可直接进入人体血液补充能量的是 ,可用作食品防腐剂的是 ,常用作食品着色剂的是 ,常用作治疗胃酸过多的抗酸剂的是 。
(2)2012年世界青年奥运会将在南京举办。保护环境,人人有责。
①空气质量监测中,不需要监测物质的浓度指标是 ,形成酸雨的物质是 。
| A.可吸入颗粒物的含量 | B.NO2 | C.SO2 | D.CO2 |
② 在处理产生的废水时,需先加入明矾,其作用是 ;后通入氯气或二氧化氯,其作用是 。
③汽车尾气需要用催化转化器减少有毒气体排放。汽车尾气中CO、NO在催化剂作用下生成可参与大 气循环的两种气体,请写出其反应方程式 。
④对垃圾需要分类处理。右图所示的垃圾分类标志的含义是 。

(3)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等。用灼烧法可初步鉴别三种纤维,给三种纤维编号后,分别灼烧产生的气味如下:
| 纤维编号 |
① |
② |
③ |
| 灼烧时的气味 |
特殊气味 |
烧纸气味 |
烧焦羽毛气味 |
则羊毛的编号为_____,棉花的编号为_______,涤纶的编号为_______。
(7分)对于反应2SO2+O2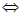 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
| 编号 |
改变的条件 |
生成SO3的速率 |
| ① |
升高温度 |
|
| ② |
降低温度 |
|
| ③ |
增大氧气的浓度 |
|
| ④ |
使用催化剂 |
|
| ⑤ |
压缩体积 |
|
| ⑥ |
恒容下充入Ne |
|
| ⑦ |
恒压下充入Ne |
已知:①FeS不溶解于水;②实验室制取H2S、SO2气体的原理是:
FeS+H2SO4=FeSO4+H2S↑ Na2SO3+H2SO4=Na2SO4+H2O+SO2↑
③硫化氢与二氧化硫气体相遇会发生反应:2H2S+SO2=3S+2H2O
根据下图中A~D的实验装置和试剂进行实验,回答下列问题:
⑴装置A是由双孔塞、玻璃导管及和组装起来的
⑵组装一套制取SO2气体的装置,并证明SO2既有氧化性、又有还原性和漂白性
①按实验装置连接顺序,把a f各导管口连接起来,正确的顺序有
f各导管口连接起来,正确的顺序有
| A.befcda | B.adcefb | C.acdfeb | D.acdefb |
②若C装置中的溶液为,反应后该溶液变为无色,说明SO2具有还原性;
③若C装置中的溶液为,反应后该溶液变为无色,说明SO2具有漂白性;
④当D中产生现象时,说明SO2具有氧化性;
(3)D装置烧杯中NaOH溶液的作用。
下图是元素周期表的框架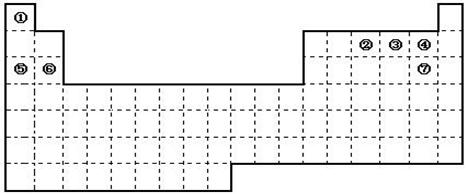
(1)请在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)依据元素周期表回答下列问题:
| A.周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是(用化学式表示)。 |
| B.周期表中的元素④和元素⑦的氢化物的熔、沸点高低顺序是(用化学式表示)。 |
| C.①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是(填写结构式)。 |
| D.在上面元素周期表中全部是金属元素的主族是;全部是非金属元素的主族是(填写字母a、b、c、d)。 |
a.ⅠA族 b. ⅡA族 c. ⅥA 族 d.ⅦA族
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式 ;
(4)请写出仅用①②④三种元素形成离子化合物的电子式_________。若用球棍模型表示①和③形成的化合物的分子结构,应该是。
⑸在120℃下1g①的单质在足量③的单质中完全燃烧,放出的热量为a kJ;请写出此条件下①的单质燃烧的热化学方程式 ;
①、③两种元素的单质已被应用于字宙飞船的燃料电池中,如图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电。
请回答:b是电池的极;a电极上的电极反应式是 。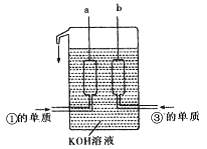
(8分)有下列八种晶体
| A.金刚石 | B.蔗糖 | C.氧化镁 | D.白磷 E.晶体氩 |
F.铝 G.水晶 H 氢氧化钠,用序号回答下列问题:
(1)只有离子键构成的化合物是 。
(2)直接由原子构成的分子晶体是 。
(3)在常温下能导电的是 。
(4)受热熔化时,需克服共价键的化合物是 。
聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域具有广泛应用。下图是利用乙酰丙酸(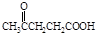 )合成聚芳酯E的路线:
)合成聚芳酯E的路线: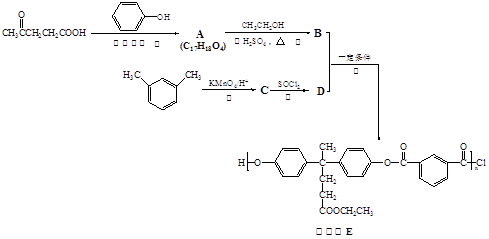
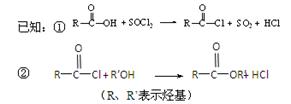
(1)乙酰丙酸中含有的官能团是羰基和(填官能团名称)。
(2)下列关于有机物A的说法正确的是(填字母序号)。
a.能发生加聚反应 b.能与浓溴水反应
c.能发生消去反应 d.能与H2发生加成反应
(3)A→B的化学方程式为。
(4)D的结构简式为。
(5)C的分子式为,符合下列条件的C的同分异构体有种。
①能发生银镜反应②能与NaHCO3溶液反应
③分子中有苯环,无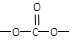 结构④苯环上只有2个取代基
结构④苯环上只有2个取代基
在上述同分异构体中,写出其中任一种与足量NaOH溶液共热反应的化学方程式:。