根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25 ℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
| pH |
<8.0 |
8.0~9.6 |
>9.6 |
| 颜色 |
黄色 |
绿色 |
蓝色 |
25 ℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为____________。
(2)向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10-10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=__________。 ②完全沉淀后,溶液的pH=__________。
③如果向完全沉淀后的溶液中继续加入50 mL 0.001 mol·L-1的盐酸,是否有白色沉淀生成?________________(填“是”或“否”)。
(3)在某温度下,Ksp(FeS)=6.25×10-18,该温度下,FeS的溶解度为 (该温度下溶液的密度为1g/mL)
Ⅰ.已知A、B、C、D四种分子所含原子的数目依次为1,3,6,6,且都含有18个电子,B、C由两种元素的原子组成,且分子中两种原子的个数比均为1:2,D是一种有毒的有机物。
(1)组成A分子的原子的元素符号是________。
(2)从B分子的立体结构判断,该分子属于________分子(填“极性”或“非极性”)。
(3)1个C分子中包含________个σ键。
(4)D的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明D是何物质):________。
Ⅱ.CO的结构可表示为CO,N2的结构可表示为NN。
(5)下表是两者的键能数据(单位:kJ·mol-1):
| A—B |
A=B |
A≡B |
|
| CO |
357.7 |
798.9 |
1071.9 |
| N2 |
154.9 |
418.4 |
941.7 |
结合数据说明CO比N2活泼的原因:________。
Ⅲ.Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关。
(6)基态Ni原子的核外电子排布式为________,基态Cu原子的价电子排布式为________。
(7)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于________(填晶体类型)。
氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为________。氧元素与氟元素能形成OF2分子,该分子的空间构型为________。
(2)根据等电子原理,在NO2+离子中氮原子轨道杂化类型是________;1 mol O22+中含有的π键数目为________个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr3+基态核外电子排布式为________。
(4)钙在氧气中燃烧时得到一种钙的氧化物晶体,其晶体结构如图所示,则该钙的氧化物的化学式为________。
(5)下列物质的分子与O3分子的结构最相似的是________。
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(6)O3分子是否为极性分子?________。
LED照明是我国制造业为人类做出的一大贡献。目前市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如下图。试回答: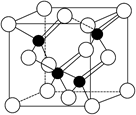
(1)镓的基态原子的电子排布式是__________。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为__________,与同一个镓原子相连的砷原子构成的空间构型为__________。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是__________。(用氢化物分子式表示)
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为__________。
(5)比较二者的第一电离能:As__________Ga(填“<”、“>”或“=”)。
(6)下列说法正确的是__________(填字母)。
| A.砷化镓晶胞结构与NaCl相同 |
| B.GaP与GaAs互为等电子体 |
| C.电负性:As>Ga |
| D.砷化镓晶体中含有配位键 |
已知烃B分子内C、H原子个数比为1∶2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系: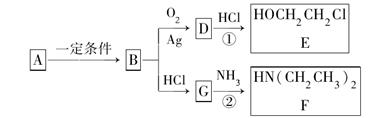
(1)B的结构简式是__________。
(2)A可能属于下列哪类物质__________。
a.醇b.卤代烃c.酚d.羧酸
(3)反应①是D与HCl按物质的量之比1∶1的加成反应,则D的分子式是__________。反应②可表示为:G+NH3―→F+HCl(未配平),该反应配平后的化学方程式为______________________。
化合物E和F是合成药品普鲁卡因的重要中间体,普鲁卡因的合成路线如下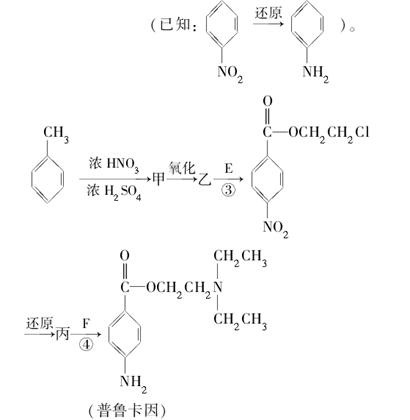
(4)甲的结构简式是__________。由甲苯生成甲的反应类型是__________。
(5)乙中有两种含氧官能团,反应③的化学方程式是____________________。
(6)普鲁卡因有两种水解产物丁和戊。
①戊与甲互为同分异构体,戊的结构简式是______________________。
②戊经聚合反应制成的高分子纤维广泛应用于通讯、宇航等领域。该聚合反应的化学方程式为______________________。
有机物A只由C、H、O三种元素组成,常用作有机合成的中间体,16.8 g该有机物经燃烧测得生成44.0 g CO2和14.4 g水,质谱图表明其相对分子质量为84;红外光谱分析表明A中含有O—H键和位于分子端的CC键,核磁共振氢谱显示有3个峰,峰面积比为6:1:1。
(1)写出A的分子式:________;
(2)写出A的结构简式:________;
(3)下列物质一定能与A发生反应的是________(填序号);
a.H2 b.Na c.KMnO4 d.Br2
(4)有机物B是A的同分异构体,1 mol B可以与1 mol Br2加成,该有机物所有碳原子在同一平面上,没有顺反异构现象,则B的结构简式为________。