如图是实验室中制备气体或验证气体性质的装置图

(1)发生装置A中制取氯气的化学方程式_________________________________。
(2)利用上图装置制备纯净的氯气,并证明氧化性:C12>Fe3+
则装置B中的溶液的作用是_______________________________________ ;
装置D中加的最佳试剂是(填序号)___________ :
供选试剂:a.浓H2SO4 b.FeCl2溶液 c.无水氯化钙 d.KSCN与FeCl2的混合溶液
(3)在上图所示圆底烧瓶内加入碳, a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具氧化性和漂白性:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的___________(填溶液名称),E中加入___________溶液(填化学式)。
(4)证明碳元素的非金属性比硅元素的强的现象为________________________________;
实验2不严谨之处应如何改进_______________________________________________。
氯气是一种重要的化工原料。
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是。
(2)资料显示:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
①在该实验中,甲部分的装置是(填字母);
②乙装置中FeCl2溶液与Cl2反应的离子方程式是。证明FeCl2与Cl2发生了氧化还原反应的实验方法是;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、清毒的物质。已知碳酸的酸性强于次氯酸则丙中反应的化学方程式是
④该实验存在明显的缺陷改进的方法是
(3)为测定漂白粉中 Ca(ClO)2的质量分数,该小组将2.0g漂白粉配制成250mL溶液,取出25mL并向其中依次加入过量稀H2SO4、过量KI溶液,完全反应后,再滴入0.1mol·L-1Na2S2O3溶液:2Na2S2O3+I2=Na2S4O6+2NaI,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为。
Ca(ClO)2的质量分数,该小组将2.0g漂白粉配制成250mL溶液,取出25mL并向其中依次加入过量稀H2SO4、过量KI溶液,完全反应后,再滴入0.1mol·L-1Na2S2O3溶液:2Na2S2O3+I2=Na2S4O6+2NaI,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为。
化学兴趣小组同学运用类比学习的思想,探究过氧化钠与二氧化硫的反应。小组同学改进了下图所示的装置进行实验。充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃。
 试回答下列问题:
试回答下列问题: (1)请你完成装置改进的措施和理由:
(1)请你完成装置改进的措施和理由: ①措施:在A、B之间加一个干燥管,
①措施:在A、B之间加一个干燥管, 理由_______________________________________
理由_______________________________________ ②措施:在B,C之间装有一个NaOH的洗气瓶,
②措施:在B,C之间装有一个NaOH的洗气瓶, 理由__________________________________
理由__________________________________ (2)某同学推断该白色固体为Na2SO3,则其所类比的化学反应是
(2)某同学推断该白色固体为Na2SO3,则其所类比的化学反应是 _______________________ (用化学方程式表示)。
_______________________ (用化学方程式表示)。 任何的推论都要经过检验,请完成对白色固体成分的探究:
任何的推论都要经过检验,请完成对白色固体成分的探究: 限选实验仪器与试剂:烧杯、试管、药匙、滴管、酒精灯、带单孔胶塞的导管、棉花、试管夹;3 mol·L-1HCl、6 mol·L-1HNO3、NaOH稀溶液、蒸
限选实验仪器与试剂:烧杯、试管、药匙、滴管、酒精灯、带单孔胶塞的导管、棉花、试管夹;3 mol·L-1HCl、6 mol·L-1HNO3、NaOH稀溶液、蒸 馏水、1 mol·L-1 BaCl2溶液、澄清石灰水、品红溶液。
馏水、1 mol·L-1 BaCl2溶液、澄清石灰水、品红溶液。
① 提出合理假设:(不需要考虑Na2O2的存在)
提出合理假设:(不需要考虑Na2O2的存在) 假设1:白色固体为Na2SO3;假设2:白色固体为Na2SO3与Na2SO4的混合物;
假设1:白色固体为Na2SO3;假设2:白色固体为Na2SO3与Na2SO4的混合物; 假设3: 。
假设3: 。
② 设计实验方案证明以上三种假设,并按下表格式写出实验操作步骤、预期现象与结论。
设计实验方案证明以上三种假设,并按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 |
预期现象与结论 |
| 步骤1: |
|
| 步骤2: |
|
对于混合物的分离或提纯,常采用的方法有:①过滤②蒸发结晶③蒸馏④萃取⑤洗气。选用合适的方法序号填空。
(1)从碘水中提取碘单质,可用方法。
(2)除去H2中的CO2,可用的方法。
(3)为了从氯化钾和二氧化锰的混合物中获得氯化钾,可先加足量的水溶解,,将得到的滤液,就可得到氯化钾晶体。
指明除去下列物质中所混有的少量杂质,应加入的试剂,写出有关反应的化学方程式。
| 试剂 |
化学方程式 |
|
| (4)FeCl2溶液中混有少量FeCl3 |
科学探究的基本程序包括形成问题、建立假设、设计研究方案、检验假设、表达或交流结果等。请根据课本中的《活动与探究》相关知识回答问题。
某同学应用如下所示装置研究气体的性质。现有某气体,其 主要成分是氯气,还含有少量空气和水蒸气。
主要成分是氯气,还含有少量空气和水蒸气。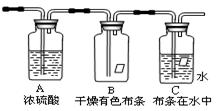
请回答:该项研究的主要目的是___。浓硫酸的作用是_ __。B、C中能观察到的实验现象是_。从物质性质方面来看,这样的实验设计方案不符合绿色化学的理念,你认为该如何改进?__ ___。
(1)实验室有一包明矾,某同学拟通过实验检验明矾中含有K+、Al3+、SO42-等3种离子。请按要求回答以下问题:
该同学将适量明矾溶于水制成溶液,并把溶液分成三份。他用第1份溶液来检验K+的操作方法是用洁净的铂丝蘸取待测溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察其焰色为色。