现有原子序数依次增大的W、T、X、Y、Z、R六种前四周期元素.TW3能使湿润的红色石蕊试纸变蓝色.X、Y位于同一主族且Y的原子序数是X的2倍.Z、R是生活中常见金属,Z、R的器皿在潮湿空气中分别生成红褐色锈和绿色锈.
请回答下列问题:
(1)TW3的电子式为 .
(2)由W、T、X、Y中的元索组成一种离子化合物M,能发生如图转化关系:

F与E的相对分子质量之差为16.则M的化学式可能为 .
C与水反应的化学方程式为 .
(3)(TW4)2Y2X8能和ZYX4在水溶液中反应生成Z2+和YX42﹣,写出离子方程式 .
(4)常温下,在WTX3浓溶液中以Z、R为电板构成原电池,负极材料是 ,
正极反应式为 .
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺。
I.火法熔炼工艺:将处理过的黄铜矿加人石英,再通人空气进行焙烧,即可制得粗铜。
(1)焙烧的总反应式可表示为:2CuFeS2 + 2SiO2+5O2=2Cu+2FeSiO3+4SO2该反应的氧化剂是。
(2)下列处理SO2的方法,不合理的是_____
A高空排放B用纯碱溶液吸收制备亚硫酸钠
C用氨水吸收后,再经氧化制备硫酸铵 D用BaCl2溶液吸收制备BaSO3
(3)炉渣主要成分有FeO 、Fe2O3 、SiO2、Al2O3等,为得到Fe2O3加盐酸溶解后,后续处理过程中未涉及到的操作有。
A过滤 B加过量NaOH溶液C蒸发结晶D灼烧 E加氧化剂
II.FeCl3溶液浸取工艺:其生产流程如下图所示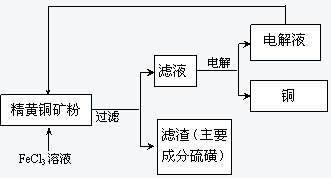
(4)浸出过程中,CuFeS2与FeCl3溶液反应的离子方程式为____________。
(5)该工艺流程中,可以循环利用的物质是____ (填化学式)。
(6)若用石墨电极电解滤液,写出阳极的电极反式_____________。
(7)黄铜矿中含少量Pb,调节C1一浓度可控制滤液中Pb2+的浓度,当c(C1一)=2mo1·L-1时溶液中Pb2+物质的量浓度为mol·L-1。[已知KSP(PbCl2)=1 x 10一5]
【有机物化学基础】
图中A、B、C、D、E、F、G均为有机化合物根据图回答问题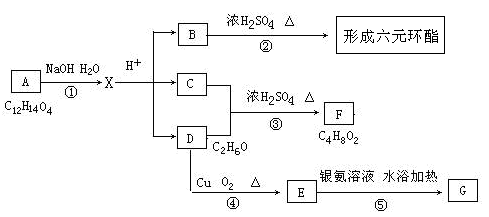
(1)A、B的相对分子质量之差是,B可能的结构简式;
(2)上述转化关系属于取代反应类型的是(用序号表示);
(3)写出反应③、⑤的化学方程式:、;
(4)B的同分异构体有多种,其中同时符合下列条件的同分异构体有种,写出其中任一种的结构简式。
①是苯环的二元取代物
②与NaHCO3反应产生无色气体
③与FeCl3溶液显紫色
化合物
是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下: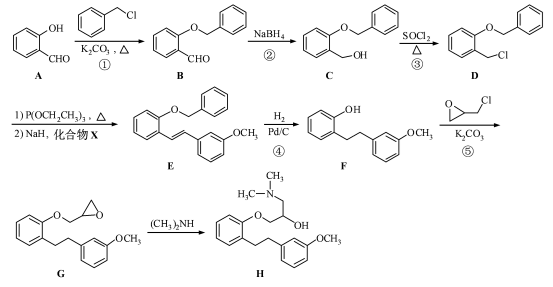
(1)化合物A 中的含氧官能团为和(填官能团名称)。
(2)反应①→⑤中,属于取代反应的是(填序号)。
(3)写出同时满足下列条件的B 的一种同分异构体的结构简式:。
I. 分子中含有两个苯环;II. 分子中有7 种不同化学环境的氢;III. 不能与
溶液发生显色反应,但水解产物之一能发生此反应。
(4)实现D→E 的转化中,加入的化合物
能发生银镜反应,
的结构简式为。
(5)已知: 。化合物
。化合物 是合成抗癌药物美法伦的中间体,请写出以
是合成抗癌药物美法伦的中间体,请写出以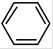 和
和 为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:。
为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:。
化合物
是合成天然橡胶的单体,分子式为
。
的一系列反应如下(部分反应条件略去):
回答下列问题:
(1)
的结构简式为,化学名称是;
(2)
的分子式为;
(3)②的反应方程式为;
(4)①和③的反应类型分别是,;
(5)
为单溴代物,分子中有两个亚甲基,④的化学方程式为;
(6)
的同分异构体中不含聚集双烯(
)结构单元的链状烃还有种,写出其中互为立体异构体的化合物的结构简式。
(15分)芳香烃M的相对分子质量为92,是一种重要的有机黄原料,某工厂以它为初始原料设计出如下合成路线图(部分产物,反应条件省略)。其中A是一氯代物。
已知:Ⅰ
Ⅱ (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与题中所给信息回答下列问题:
(1)M的结构简式是;M→A的反应条件是。
(2)A中的共面原子最多个。
(3)写出反应④的化学山程式。
(4)②的反应类型属于;②和③的反应顺序(填“能”或“不能”)颠倒。
(5) 有多种同分异构体,写出2种含有1个醛基和2个羟基,苯环上只能生成2种一氯取代物的芳香族化合物的结构简式: 。
有多种同分异构体,写出2种含有1个醛基和2个羟基,苯环上只能生成2种一氯取代物的芳香族化合物的结构简式: 。
(6)写出由A转化为 的合成路线(用
的合成路线(用 表示,并在箭号上写明反应试剂及反应条件)。
表示,并在箭号上写明反应试剂及反应条件)。