(现有以下物质:①NaOH溶液 ②液氨 ③BaCO3固体 ④熔融KHSO4 ⑤Fe(OH)3胶体 ⑥铜⑦CO2 ⑧CH3COOH
(1)以上物质中属于混合物的是____________(填序号)
以上物质中属于非电解质的是____________(填序号)
(2)对物质⑤进行通电,观察到阴阳两极的现象是____________
以上纯净物中能导电的是___________(填序号)
(3)写出①和⑧的水溶液反应的离子方程式____________
(4)写出④的电离方程式____________
(5)在足量④的水溶液中加入少量③,发生反应的离子方程式为____________
(6)在含0.4mol①的溶液中缓慢通入标准状况下6.72LCO2,气体被完全吸收,则反应后的溶质有___________(填化学式),该过程总的离子反应方程式为____________
(6 分)从Ca、C 、S、H、O 、N六种元素中选择适当的元素按要求填空。
(1)人体中元素含量最高的是 __________ ;
(2)常用作干燥剂的一种酸_____________;(填化学式,下同)。
(3)能作为燃料的有机化合物是__________:
(4)既可用来消毒杀菌,又可用来改良酸性土壤的碱是__________;
(5)造成煤气中毒的是__________。
(6)绿色植物进行光合作用吸收的是________________;
A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体、B为黄绿色气体、C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体。它们之间的转化关系如图所示(其中某些反应条件和部分反应产物已略去)。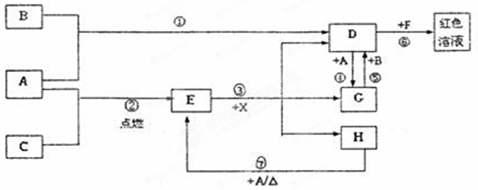
(1)写出下列物质的化学式:D X 。
(2)在反应①~⑦中,不属于氧化还原反应的是(填编号)。
(3)反应⑥的离子方程式为:。
(4)往G溶液中加入NaOH溶液观察到的现象是。
(5)反应⑦的化学方程式为;该反应中每消耗0.3mol的A,可转移电子mol。
(6)除去D溶液中混有的少量G的方法是:
(7)在D溶液中制备无水D的方法是:
(8)分别写出D溶液与小苏打溶液反应的离子方程式是:
甲乙两位同学分别用不同的方法配制100 mL 3.6 mol·L-1的稀硫酸。
(1)若采用18 mol·L-1的浓硫酸配制溶液,需要用到浓硫酸的体积为__________。
(2)甲学生:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶中加水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①将溶液转移到容量瓶中的正确操作是________________________________。
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是__________________。
③定容的正确操作是___________________________________________________。
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度线,处理的方法是________(填序号)。
| A.吸出多余液体,使凹液面与刻度线相切 |
| B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切 |
| C.经计算加入一定量的浓硫酸 |
| D.重新配制 |
(3)乙学生:用100 mL量筒量取浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加水至100 mL刻度线,搅拌均匀,你认为此法是否正确?若正确,不用解释原因;若不正确,指出其中错误之处______________________ _ ______
_______________________。
某淡黄色的颗粒状固体,其化学性质比较活泼,在通常状况下能跟许多物质发生化学反应。例如:它与CO2反应时,只生成了Na2CO3和O2,它与稀盐酸反应时,只生成了NaCl、H2O和O2。上课时,老师做了如下实验:
a.取少量的淡黄色的颗粒状固体投入到盛有少量水的试管中,可观察到产生了一种无色无味的气体;
b.再向试管中滴加几滴酚酞试液,可观察到烧杯中溶液变红。
根据实验现象,回答下列问题:
(1)淡黄色的颗粒状固体中一定含有元素。你做出这个判断的理由是。
(2)实验a中产生的气体,可用法收集。
(3)同学们对实验a中产生的气体的组成看法不一,提出了以下几种假设:
①该气体是CO;②该气体是H2。
请你推测该气体还可能是(写化学式)。
(4)设计一个实验,证明你在(3)中的推测(写出简要操作步骤,反应现象和结论)。
| 操作步骤 |
|
| 反应现象 |
|
| 结论 |
某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含SO2的废气和含H2SO4的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。
(1)分析该镇下酸雨的原因:
(2)举一例说明酸雨对环境造成的危害:
(3)该镇某中学环保小组提出了治理酸雨的下列措施,你认为其中不妥的是
| A.将硫酸厂搬离该镇 | B.建议环保部门限令整改 |
| C.将硫酸厂排出的废气中的SO2处理后排放 | D.工厂和居民改用较清洁的燃料 |
(4)可用熟石灰来处理硫酸厂排出的酸性废水,处理原理的化学方程式是
(5)浓硫酸弄到手上后应立即用水冲洗,然后涂上碳酸氢钠。若是稀硫酸弄到手上,
(填“需要”或“不需要”)这样做,理由是