现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵,⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号) 。
(3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 。
(4)已知t℃,KW=1×10-13,在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= 。
在 H,
H, H,
H,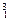 H,
H,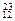 Mg,
Mg,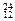 Mg,
Mg,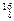 O,
O, O,
O, O中
O中
(1)共有______种元素,______种原子,中子数最多的是。
D218O的相对分子质量是______。
(2)和互为同位素
和的质量数相等,但不能互称同位素
和的中子数相等,但质子数不等,所以不是同一种元素
在含有Cl-.Br-.I- 的溶液中,已知其浓度均为0.1 mol/L,而AgCl.AgBr.AgI的浓度积(mol2/L2)分别为:1.6×10-10.4.1×10-15.1.5×10-16。若向混合溶液中逐滴加入AgNO3溶液并充分搅拌时,首先析出的沉淀是_______________,最后析出的沉淀是_________;当AgBr沉淀开始析出时,溶液
的溶液中,已知其浓度均为0.1 mol/L,而AgCl.AgBr.AgI的浓度积(mol2/L2)分别为:1.6×10-10.4.1×10-15.1.5×10-16。若向混合溶液中逐滴加入AgNO3溶液并充分搅拌时,首先析出的沉淀是_______________,最后析出的沉淀是_________;当AgBr沉淀开始析出时,溶液 中Ag+的浓度是___________________
中Ag+的浓度是___________________
反应3Fe(S)+4H 2O==Fe3O4(s)+4H2(g),在
2O==Fe3O4(s)+4H2(g),在 一可变的容积的密闭容器中进行,试回答:
一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是(填增大、不变、减 小,以下相同)
小,以下相同)
②将容器的体 积缩小一半,其正反应速率,逆反应速率
积缩小一半,其正反应速率,逆反应速率 。
。
③保持体积不变,充入N2使体系压强增大,其正反应速率,逆反应速率。
④保持压强不变,充入N2使容器的体积增大,其正反应速率,逆反应速率。
目前世界上比较先进的电解制碱技术是离子交换法,如图为离子交换膜法电解饱和食盐水的原理示意图。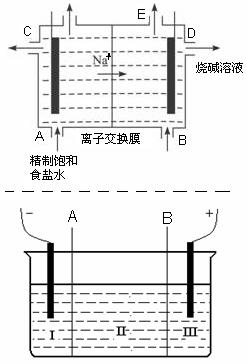
(1)下列说法不正确的是
| A.从E口逸出的气体是H2 |
| B.从B口加入含少量NaOH的水溶液以增强导电性 |
| C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH |
| D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加 Na2CO3溶液 |
(2)现有离子交换膜A和B将电解槽分为I、II、III三个区域(下图所示),在这种电解池中电解Na2SO4溶液可 制得氢氧化钠、硫酸等物质。A为离子交换膜、B为离子交换膜(填“阴”或“阳”),电极均为惰性电极。Na2SO4溶液应该在区(填“I”、“II”、“III”)加入。通电电解时阴极的电极反应式为
制得氢氧化钠、硫酸等物质。A为离子交换膜、B为离子交换膜(填“阴”或“阳”),电极均为惰性电极。Na2SO4溶液应该在区(填“I”、“II”、“III”)加入。通电电解时阴极的电极反应式为 ,在III区得到。当外电路总共通过30 mol电子时,生成的NaOH 960克,则电解过程中能量的转化率为:
,在III区得到。当外电路总共通过30 mol电子时,生成的NaOH 960克,则电解过程中能量的转化率为:
Ⅰ、A物质的化学式为M(OH)2,将其溶于水制成稀溶液,该溶液呈中性,在溶液中存在:
M2+ + 2OH-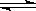 M(OH)2
M(OH)2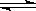 2H+ + MO22-
2H+ + MO22-
回答以下题目一律用“增大”“减小”“不变 ”填空
”填空
(1)在其他条件不变的情况下,25Co时,在蒸馏水中加入A物质后,与加入前比较,
①由水电离出的C(OH-),C(H+),水的电离度,Kw
(2)25Co时,向A的稀溶液中加入少量的烧碱固体。
则水的电离度,溶液的pH
Ⅱ、.室温下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中C(OH-)之比为10 (填大于、等于或小于)