根据下表中烃的分子式排列规律,判断空格中烃的同分异构体的数目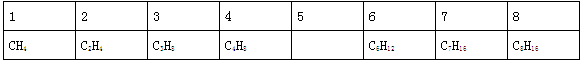
| A.3 | B.4 | C.5 | D.6 |
将Cl2与SO2混合均匀后,分别通入到少量下列溶液中,溶液颜色一定会褪去的是
| A.I2与淀粉混合溶液 | B.KMnO4溶液 | C.品红溶液 | D.紫色石蕊试剂 |
海洋中资源丰富,如下图所示,下列有关说法正确的是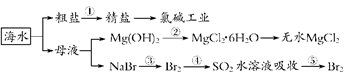
| A.工段③④⑤是溴元素的富集过程,③④⑤中均发生了氧化还原反应 |
| B.工段②中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2 |
| C.氯碱工业通过电解NaCl溶液,主要生产Cl2、H2和纯碱 |
| D.工段①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,操作顺序为:加入足量BaCl2溶液→加入足量NaOH溶液→加入足量Na2CO3溶液→加入足量盐酸→过滤 |
含有1mol HNO3的稀硝酸分别与不同物质的量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断正确的是
| A.a是Fe(NO3)2 | B.n1=0.375 | C.p=0.20 | D.n2=0.30 |
下列离子方程式书写正确的是
| A.用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+= Cu2++2H2O |
B.实验室制氯气:MnO2+4HCl(浓)  Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| C.用FeS除去工业废水中的Hg2+:Hg2++S2-=HgS↓ |
| D.向次氯酸钠溶液中通入少量二氧化硫:ClO-+ SO2 + H2O = Cl-+SO42- + 2H+ |
已知:Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反,I2的氧化性比S强。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是
| A.Fe2S3和 Al(OH)3 | B.Fe(OH)3和Al(OH)3 |
| C.FeS、Al(OH)3和S | D.Al2S3、FeS和S |