向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成,经查资料得知:
Ag++2NH3•H2O Ag(NH3)2++2H2O下列分析不正确的是
Ag(NH3)2++2H2O下列分析不正确的是
A.浊液中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
| B.实验表明实验室可用氨水洗涤银镜反应后的试管 |
| C.实验可以证明NH3结合Ag+能力比Cl--强 |
| D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |
2011国际化学年瑞士发行了一枚印有维生素C(只含C、H、O三种元素)分子球棍模型的邮票,以纪念化学家Reichstein1933年首先合成维生素C。下列关于维生素C的说法正确的是
A.维生素C的分子式C6H10O6
B.维生素C不能使酸性高锰酸钾褪色
C.维生素C分子含有两个手性碳原子
D.1mol维生素C与足量的钠反应能产生2molH2
向50mL 稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应。下列说法正确的是
| A.开始时产生的气体为H2 |
| B.AB段发生的反应为置换反应 |
| C.所用混合溶液中c(HNO3)="0.5" mol·L—1 |
| D.参加反应铁粉的总质量m2=5.6g |
工业上可用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制取干电池中所需的MnO2和Zn,其工艺流程如下:
下列说法正确的是
| A.酸溶时,MnO2作还原剂 | B.可用盐酸代替硫酸进行酸溶 |
| C.原料硫酸可以循环使用 | D.在电解池的阴极处产生MnO2 |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1L0.1mol·L—1的氨水中含有的NH3分子数为0.1NA |
| B.标准状况下,2.24L的CCl4中含有的C—Cl键数为0.4NA |
| C.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4 NA |
| D.常温常压下,Na2O2与足量CO2反应生成2.24L O2,转移电子数为0.2NA |
下列有关实验装置的说法中正确的是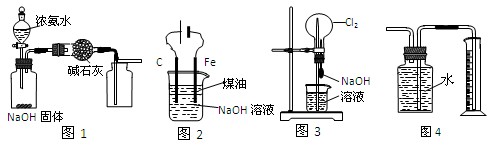
| A.用图1装置制取干燥纯净的NH3 |
| B.用图2装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.用图3装置可以完成“喷泉”实验 |
| D.用图4装置测量Cu与浓硝酸反应产生气体的体积 |