200℃时,11.6g由CO2和H2O组成的混合气体与足量的Na2O2充分反应后,固体质量增加3.6g,则原混合气体的平均相对分子质量为
| A.5.8 | B.11.6 | C.23.2 | D.46.4 |
下列叙述正确的是
| A.食用白糖的主要成分是蔗糖 |
| B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一反应类型 |
| C.乙醇、乙烷和乙酸都可以与钠反应生成氢气 |
| D.淀粉、油脂和蛋白质都是高分子化合物 |
氢气是一种高能、清洁的能源,且是重要的工业原料。煤的气化过程存在如下反应:
CO(g)+ H2O(g)  CO2(g) + H2(g) △H <0
CO2(g) + H2(g) △H <0
反应达到平衡后,采用如下措施可提高CO转化率的是
| A.更换高效催化剂 | B.增大CO 的浓度 | C.降低温度 | D.增大压强 |
已知A、B为单质,C为化合物,A、B、C存在如下转化关系: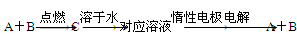
则下列叙述正确的是
①若C溶于水后得到强碱溶液,则A可能是Na,B可能是O2
②若C的溶液遇Na2CO3,放出CO2气体,则A可能是H2,B可能是Cl2
③若C的溶液中滴加KSCN溶液显红色,则A可能是Fe,B可能为Cl2
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则A可能是Cu,B可能为Cl2
A.①② B.②④ C.①③ D.③④
在密闭容器中,反应X2(g)+2Y2(g) 2X Y2(g) ΔH<0达到甲平衡,若只改变某一条件再达到乙平衡,则对此过程条件改变的分析正确的是
2X Y2(g) ΔH<0达到甲平衡,若只改变某一条件再达到乙平衡,则对此过程条件改变的分析正确的是
| A.图Ⅰ由甲至乙加入适当催化剂 | B.图Ⅱ由甲至乙扩大容器体积 |
| C.图Ⅲ由甲至乙增大压强 | D.图Ⅲ由甲至乙升高温度 |
已知:
(1) 2Fe(s)+O2(g) =2FeO(s) △H=-544kJ·mol-1
(2) 2Al(s)+3/2 O2(g) =Al2O3(s) △H=-1675kJ·mol-1
则 2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H为
| A.-2491 kJ·mol-1 | B.+859 kJ·mol-1 |
| C.-1403 kJ·mol-1 | D.-859 kJ·mol-1 |