下列除去杂质的方法正确的是
① 除去乙烷中少量的乙烯:通入酸性高锰酸钾溶液中;
② 除去乙酸乙酯中的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏;
③ 除去苯中少量的苯酚:加入足量浓溴水后过滤;
④ 除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
| A.② ④ | B.② ③ | C.②③④ | D.全部正确 |
有一铁粉和氧化铜的混合物6.96g,进行如下实验: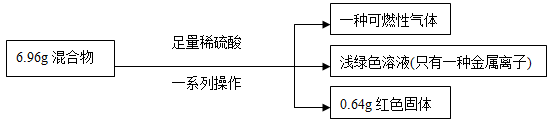
根据实验所得数据,关于混合物相关说法正确的是
| A.生成气体质量为0.2g |
| B.原混合物中铁的质量分数无法计算 |
| C.实验中反应的H2SO4质量为10.78g |
| D.原混合物中铜元素的质量不一定为0.64g |
下列说法正确的是
| A.最外层电子排布为ns2的元素一定处于周期表IIA族 |
B.主族元素X、Y能形成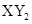 型化合物,则X与Y 的原子序数之差可能为2或5 型化合物,则X与Y 的原子序数之差可能为2或5 |
| C.亚硫酸的酸性比硫酸强 |
| D.金属元素的电负性一定比非金属元素的电负性大 |
含有a mol FeBr2的溶液中,通入 x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
| A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl- |
| B.x=0.6a,2Br-+Cl2=Br2+2Cl- |
| C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- |
| D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- |
以下反应中不属于氧化还原反应的是
| A.2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O |
| B.2Na2O2+2H2O=4NaOH+O2↑ |
| C.FeO+4HNO3(浓)=Fe(NO3)3+NO2↑+2H2O |
| D.Mg(HCO3)2+4NaOH=Mg(OH)2↓+2Na2CO3+2H2O |
设阿伏加德罗常数的数值为6.02×l023,下列叙述错误的是()
①电解法精炼铜时转移的电子数为6.02×l023时,阳极溶解32 g铜
②7.8 g Na2S和Na202的混合物中,含有的阴离子数大于0.1×6.02×l023
③在适当条件下,2 mol S02和1 mol 02充分反应后,容器内的分子数大于2×6.02×l023
④2.9 克 2CaS04.H20含有的结晶水分子数为0.02×6.02×l023(2CaS04.H20相对分子质量为290)
⑤含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1×6.02×l023
| A.①②③④⑤ | B.①③④⑤ | C.①②④⑤ | D.②③④⑤ |