在热的稀硫酸中溶解了11.4 g FeSO4固体,当加入50 mL 0.5 mol·L-1 KNO3溶液时,其中的Fe2+全部转化成Fe3+,KNO3也完全反应并放出NxOy气体。
(1)推算出x=________;y=________。
(2)配平该反应的方程式:
____FeSO4+___KNO3+____H2SO4 = ____K2SO4+____Fe2(SO4)3+____ (NxOy)+____H2O(配平时x、y用具体数值表示,物质填在
(NxOy)+____H2O(配平时x、y用具体数值表示,物质填在 中)。
中)。
(3)反应中氧化产物是__________。
⑴加热10.0g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45g,求混合物中碳酸钠的质量分数。(列出计算过程)
⑵过氧化钠与铝粉混合物共18.3g,加入100ml 水,充分反应后混合物完全溶解,并收集到5.6L气体(标准状况).则收集到的气体成份是,体积比是。
某课外活动小组设计了如下图所示的实验装置进行实验。回答下列问题: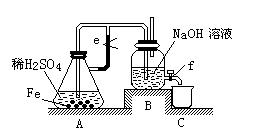
⑴ 开始实验时弹簧夹e是打开的,A中发生反应的离子方程式为:,B中可以观察到的现象是。
⑵ 数分钟后夹上弹簧夹e,B中可以观察到的现象是。
⑶ 如果开启活塞f放掉2/3液体,B中可观察到的现象是,
有关反应的化学方程式是
物质有以下转化关系: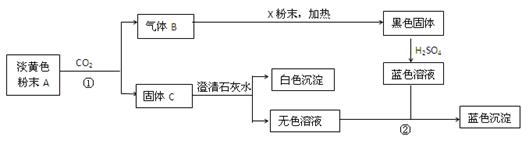
根据上图和实验现象,回答下列问题:(用化学式表示)
(1)A是,B是,C是,X粉末是。
(2)写出反应①的化学方程式。
(3)写出反应②的离子方程式。
某无色透明溶液,投入金属铝可放出H2。现有下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、
HCO3-、OH-。试判断下列两种情况时,各有哪些离子可存在于此溶液中:
(1)当生成Al3+时,可存在的离子有;
(2)当生成AlO2-时,可存在的离子有。
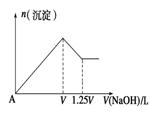
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则溶液中MgCl2与
Al2(SO4)3的物质的量浓度之比为 ___________