下列实验设计方案中,可行的是
| A.用加入适量铁粉的方法除去Cu(NO3)2溶液中混有的AgNO3 |
| B.用盛有NaOH溶液的洗气瓶除去CO2中混有的HCl气体 |
| C.向某无色未知溶液中加入BaCl2溶液,检验未知溶液中的SO42- |
| D.用加热的方法提纯含有少量碳酸氢钠的碳酸钠 |
已知铜与稀硫酸不发生反应,但如果在铜与稀硫酸的混合溶液中加入某种盐,就能发生反应,且有气体、有沉淀产生,则该盐是
| A.FeCl3 | B.Ba(NO3)2 | C.Na2SO4 | D.KCl |
检验SO2中是否混有CO2气体,可采用的方法是
| A.通过品红溶液,若品红溶液褪色,则说明混有CO2气体 |
| B.通过澄清石灰水,若变混浊,则说明混有CO2气体 |
| C.先通过足量NaOH溶液,再通过澄清石灰水,若变混浊,则说明混有CO2气体 |
| D.先通过足量KMnO4溶液(具有强氧化性),再通过澄清石灰水,若变混浊,则说明混有CO2气体 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均减小 |
| D.产生气泡的速度甲比乙快 |
某金属能和盐酸反应生成氢气,该金属与锌组成原电池时,锌为负极,该金属可能为
| A.铝 | B.铜 | C.锡 | D.硅 |
可逆反应:2NO2(g)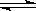 2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成nmol O2的同时生成2nmol NO2
②单位时间内生成nmol O2的同时生成2nmol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变⑤混合气体的密度不再改变
| A.①④ | B.②③⑤ | C.①③④ | D.①②③④⑤ |