为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是( )

| A.C2H5OH | B. |
| C.CH3CH2CH2COOH | D. |
化学平衡状态I、II、III的相关数据如下表:
| 编号 |
化学方程式 |
平衡常数 |
温度 |
|
| 979K |
1173K |
|||
| I |
Fe(s)+CO2(g)  FeO(s)+CO(g) FeO(s)+CO(g) |
K1 |
1.47 |
2.15 |
| Ⅱ |
CO(g)+H2O(g)  CO2(g)+H2(g) CO2(g)+H2(g) |
K2 |
1.62 |
b |
| Ⅲ |
Fe(s)+H2O(g)  FeO(s)+H2(g) FeO(s)+H2(g) |
K3 |
a |
1.68 |
根据以上信息判断,下列结论错误的是
A.a>b
B.增大压强,平衡状态II不移动
C.升高温度平衡状态III向正反应方向移动
D.反应II、III均为放热反应
某温度下在容积不变的密闭容器中发生如下反应:2SO2+O2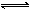 2SO3(g),若开始时只充入2 molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为
2SO3(g),若开始时只充入2 molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为
| A.20% | B.40% | C.50% | D.60% |
在容积不变的密闭容器中,在一定条件下发生反应:2A(?) B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
| A.若正反应为吸热反应,则A为非气态 |
| B.若正反应为放热反应,则A为气态 |
| C.若在平衡体系中加入少量C,则该平衡不移动 |
| D.压强对该平衡的移动无影响 |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001 mol/(L·s) |
B.容器体积变为20 L,Z的平衡浓度变为原来的 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的△H>0 |
下图中a曲线表示一定条件下可逆反应 X(g)+Y(g)====2Z(g)+W(s) △H<0的反应过程。若使a曲线变为b曲线,可采用的措施是
| A.升高温度 | B.增大Y的浓度 |
| C.降低温度 | D.增大体系压强 |