已知:2BrO3-+Cl2=Br2 +2ClO3-;5Cl2 +I2 +6H2O =2HIO3 +10HCl;
ClO3-+5Cl-+6H+ =3Cl2+3H2O判断下列物质氧化能力强弱顺序为
| A.ClO3->BrO3->IO3->Cl2 | B.BrO3->Cl2>ClO3->IO3- |
| C.BrO3->ClO3->Cl2>IO3- | D.Cl2>BrO3->ClO3->IO3- |
 kJ
kJ 。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是
。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是
| A.前25min内反应放出的热量为46.lkJ |
| B.第25min改变的条件是将NH3从反应体系中分离出去 |
| C.若第60min时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D.若时段I中投入物质的浓度为原来的2倍,则反应物的转化率增大,平衡常数不变 |
下列说法正确的是
| A.向AgCl悬浊液中加入少量NaCl固体后振荡,c(Cl-)增大,KsP (AgCl)增大 |
B.某溶液中由水电离出的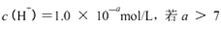 时,则该溶液的pH一定为14-a 时,则该溶液的pH一定为14-a |
| C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后溶液的pH等于7,则混合溶液 中: 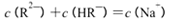 |
D.相同物质的量浓度的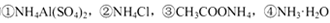 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④ 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④ |
生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池。其工作原理如图所示。下列有关说法正确的是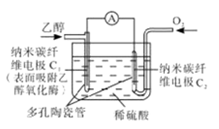
| A.O2在C2电极上得电子,被氧化 |
| B.电子由C2极经外电路流向C1极 |
| C.每转移6mole-,理论上生成22.4LCO2 |
| D.C1极的电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+ |
在盛有足量M的体积可变的密闭容器中加入N,发生反应:M (s) +2N (g)==4P (s) +Q (g) ΔH< 0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是
| A.平衡是N的转化率为50% |
| B.当温度升高后,则图中θ>450 |
| C.若再加入N,则正、逆反应速率均逐渐增大 |
| D.若再加入N,则反应体系中气体密度减小 |
已知X,Y声是元素周期表中前20号元素:|x-y|="3," X, Y能形成化合物M,下列说法正
确的是
| A.若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B.若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C.若M属于共价化合物,则该分子中原子个数比可能为1:2 |
| D.若M属于离子化合物,则该化合物中只存在离子键 |