今有如下三个热化学方程式:
H2(g)+1/2O2(g)═H2O(g)△H="a" kJ•mol-1
H2(g)+1/2O2(g)═H2O(l)△H="b" kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H="c" kJ•mol-1
关于它们的下列表述,正确的是
| A.它们都是吸热反应 | B.氢气的燃烧热为△H=akJ•mol-1 |
| C.反应热的关系:a=b | D.反应热的关系:2b=c |
关于Fe(OH)3胶体的说法正确的是
| A.属悬浊液 | B.分散质是水 |
| C.能产生丁达尔效应 | D.可完全电离成Fe3+和OH- |
分类是学习和研究化学的一种的重要方法,下列分类合理的是
| A.K2CO3和K2O都属于盐 | B.H2SO4和HNO3都属于酸 |
| C.KOH和Na2CO3都属于碱 | D.Na2O和Na2SiO3都属于氧化物 |
向某溶液中加入稀HNO3酸化的BaCl2溶液,有白色沉淀产生。该溶液含有
| A.CO32― | B.OH― | C.SO42― | D.HCO3― |
下列实验操作错误的是
A.加热盛有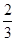 体积K2 SO4溶液的试管 体积K2 SO4溶液的试管 |
| B.用胶头滴管滴加少量NaC1溶液 |
| C.用药匙取用少量Na2SO4固体 |
| D.用10 mL量筒量取8 mL1. 0 mol.L-1 NaOH溶液 |
对元素周期表和元素周期律的发现有突出贡献的科学家是
| A.拉瓦锡 | B.阿伏加德罗 | C.门捷列夫 | D.道尔顿 |