甲、乙、丙、丁是原子序数依次增大的四种短周期元素,A、B、C、D、E是由其中的两种或三种元素组成的化合物,F是由丙元素形成的单质。已知:A+B=D+F,A+C=E+F; 0.1mol•L-1D溶液的pH为13(25℃).下列说法正确的是
A.原子半径:丁>丙>乙>甲
B.1mol A与足量B完全反应共转移了2mol电子
C.丙元素在周期表中的位置为第二周期第ⅣA族
D.由甲、乙、丙、丁四种短周期元素组成的盐,其水溶液既有呈酸性的,也有呈碱性的
下图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是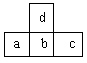
| A.a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a |
| B.d的氢化物比b的氢化物稳定 |
| C.d与c不能形成化合物 |
| D.原子半径的大小顺序是a>b>c>d |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.常温常压下1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| C.18 g D2O含有NA个质子 |
| D.0.5 mol·L-1硫酸钾溶液中阴离子所带电荷数为NA |
25 ℃时,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Na+、K+、MnO4-、CO32- |
| B.常温下c(H+)=1×10-13 mol·L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- |
| C.加入铝粉产生氢气的溶液:Na+、K+、SO42-、HCO3- |
| D.透明溶液中:K+、Cu2+、Cl-、NO3- |
下列离子方程式书写正确的是
A.醋酸溶解鸡蛋壳:2H++ CO32- CO2↑+ H2O CO2↑+ H2O |
B.铝片加入烧碱溶液:2A1+ 2OH-+ 2H2O 2A1O2-+ 3H2↑ 2A1O2-+ 3H2↑ |
C.铁与盐酸反应:2Fe+ 6H+ 2Fe3+ + 3H2↑ 2Fe3+ + 3H2↑ |
D.铜片投入FeCl3溶液中:Cu+ Fe3+ Cu2+ + Fe2+ Cu2+ + Fe2+ |
某溶液中含有下列六种离子:①HCO3- ②SO32- ③Na+ ④CO32- ⑤NH4+ ⑥NO3-,向其中加入一定量Na 2O2后,溶液中离子浓度基本保持不变的是
| A.只有⑥ | B.④⑥ | C.③④⑥ | D.①②⑤ |