窒温时,0.1 mol•L-1某一元酸HA在水中有0.1%发生电离,叙述错误的是( )
| A.该溶液的pH=4 |
| B.升高温度,溶液的pH增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列实验操作错误的是
| A.用蒸馏的方法分离汽油和煤油 |
| B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.浓硫酸稀释时,应将浓硫酸慢慢加到水中,及时搅拌并冷却 |
| D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2 |
包装危险品时,常贴上一些图标用来提醒人们。下列是一些常见危险品的图标,装运酒精时应贴的图标是
N2O5是一种新型硝化剂,其性质和制备受到人们的关注。一定温度下,在2 L固定容积的密闭容器中发生反应: 2N2O5(g) 4NO2(g) + O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中正确的是
4NO2(g) + O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中正确的是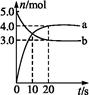
| A.0~20 s内平均反应速率v(N2O5) =" 0.1" mol·(L·s)-1 |
| B.曲线a表示NO2的物质的量随反应时间的变化 |
| C.10 s时,正、逆反应速率相等,达到平衡 |
| D.20 s时,正反应速率大于逆反应速率 |
MOH强碱和等体积、等浓度的HA弱酸溶液混合后,溶液中以下关系不正确的是
A.c(M+) > c(A-) > c(OH-) > c(H+)
B.c(HA) + c(H+) = c(OH-)
C.c(M+) > c(A-) > c(H+) > c(OH-)
D.c(M+) = c(A-) + c(HA)
2.0 mol PCl3和1.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应PCl3(g) + Cl2(g)  PCl5(g),达平衡时,PCl5为0.40 mol,如果此时移走1.0 mol PCl3和0.50 mol Cl2,在相同温度下再达平衡时,PCl5的物质的量是
PCl5(g),达平衡时,PCl5为0.40 mol,如果此时移走1.0 mol PCl3和0.50 mol Cl2,在相同温度下再达平衡时,PCl5的物质的量是
| A.0.40 mol | B.0.20 mol |
| C.小于0.20 mol | D.大于0.20 mol,小于 0.40 mol |