100℃,Kw=1.0×10-12,若在此温度时,某溶液中的c(H+)=1.0×10-7 mol•L-1,则该溶液
| A.呈中性 | B.呈碱性 |
| C.呈酸性 | D.1000c(H+)=c(OH-) |
下列化学用语正确的是
| A.苯的最简式 C6H6 | B.丙烷分子的比例模型: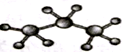 |
| C.乙烯的结构简式CH2CH2 | D.甲醛的结构式: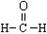 |
甲烷是以碳原子为中心的正四面体结构,而不是正方形的平面结构,其理由是
| A.甲烷中的四个键的键长、键角相等 | B.一氯甲烷只有一种结构 |
| C.二氯甲烷只有一种结构 | D.三氯甲烷只有一种结构 |
在2 KMnO4 + 16HCl ="==" 2MnCl2 + 5Cl2↑+ 8H2O + 2KCl的反应中,氧化剂和还原剂的物质的量之比是
KMnO4 + 16HCl ="==" 2MnCl2 + 5Cl2↑+ 8H2O + 2KCl的反应中,氧化剂和还原剂的物质的量之比是
| A.1﹕8 | B.8﹕1 | C.1﹕5 | D.5﹕1 |
在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比为8:1:2,则配制该溶液时所用Na2SO4、NaCl、NaOH的物质的量比为
| A.1:1:1 | B.1:4:2 | C.1:2:4 | D.1:3:2 |
下列各组离子在水溶液中能大量共存的是
| A.Na+、Ba2+、Cl-、SO42─ | B.Ca2+、HCO3-、C1-、K+ |
| C.Mg2+、Ag+、NO3-、Cl- | D.H+、 Cl-、Na+、CO32- Cl-、Na+、CO32- |