一定温度下,在一个容积为1 L的密闭容器中,充入1 mol H2(g)和1 mol I2(g),发生反应H2(g)+I2(g) 2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2L的密闭容器中充入1 mol HI(g)发生反应HI(g)
2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,在该温度下,在另一个容积为2L的密闭容器中充入1 mol HI(g)发生反应HI(g)
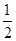 H2(g)+
H2(g)+ 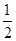 I2(g),则下列判断正确的是
I2(g),则下列判断正确的是
| A.后一反应的平衡常数为1 |
| B.后一反应的平衡常数为0.5 |
| C.后一反应达到平衡时,H2的平衡浓度为0.25 mol·L-1 |
| D.后一反应达到平衡时,HI(g)的平衡浓度为0.5 mol·L-1 |
对下列化学用语或化学原理的理解和描述均正确的是( )
A.电子式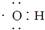 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
B.比例模型 可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 |
| C.明矾能水解生成Al(OH)3胶体,可用作饮用水杀菌 |
D.原子结构示意图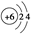 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
化学实验设计或实际操作或储存时,能体现“经济、高效、环保、安全”方案是( )
| A.Na 着火可以使用泡沫灭火器 |
| B.绿色化学是指有毒气体尾气要经过无毒处理后在排放 |
| C.实验室用浓硫酸溶解铜制备硫酸铜 |
| D.实验室可以适当温度下,使铜片在持续通入空气的稀硫酸中溶解的方法制备硫酸铜 |
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g) zC(g),达到平衡时,测得A的浓度为0.5 mol/L,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测的A的浓度降低为0.3 mol/L,下列有关判断正确的是( )
zC(g),达到平衡时,测得A的浓度为0.5 mol/L,在温度不变的条件下,将容器的体积扩大到两倍,使再达到平衡,测的A的浓度降低为0.3 mol/L,下列有关判断正确的是( )
| A.x+y<z | B.平衡向正反应方向移动 |
| C.C的体积分数下降 | D.B的浓度增大 |
8.34 g FeSO4·7H2O样品在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。下列说法中正确的是( )
| A.温度为78℃时固体物质M的化学式为FeSO4·5H2O |
| B.温度为159℃时固体物质N的化学式为FeSO4·3H2O |
C.在隔绝空气条件下由N得到P的化学方程式为FeSO4 FeO+SO3↑ FeO+SO3↑ |
| D.取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:
CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法不正确的是( )
| A.检测时,电解质溶液中的H+向正极移动 |
| B.若溶液中有0.4 mol电子通过,则在标准状况下消耗4.48 L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH+O2==CH3COOH+H2O |
| D.正极上发生的反应为:O2+4e-+4H+=2H2O |