在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不正确的是
| A.白色沉淀不含BaSO3 | B.溶液的酸性减弱 |
| C.白色沉淀是BaSO4 | D.FeCl3全部被还原为FeCl2 |
X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述不正确的是
| A.X与Y能形成两种常见的气态化合物 |
| B.原子半径的大小顺序:r(Z)>r(R)> r(X)>r(Y) |
| C.X、Z分别与R形成的化合物中化学键类型不同 |
| D.含有Y、Z、R三种元素的化合物最多只有2种 |
100mL浓度为2mol·L-1的盐酸溶液跟过量的锌片反应,为减慢反应速率,又不影响生成H2的总量,可采用的方法有
| A.加适量6mol·L-1HCl溶液 |
| B.加数滴CuCl2溶液 |
| C.加适量醋酸钠固体 |
| D.加适量NaNO3溶液 |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列说法不正确的是
| A.在熔融电解质中,O2-向负极定向移动 |
| B.电池的总反应是:2C4H10+13O2===8CO2+10H2O |
| C.通入空气的一极是正极,电极反应为:O2+4e-===2O2- |
| D.通入丁烷的一极是负极,电极反应为:C4H10 +26e-+13O2-=== 4CO2↑+5H2O |
有关实验的叙述,正确的是
| A.将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
| B.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
| C.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| D.读取滴定管内液体的体积,俯视读数导致读数偏小 |
下列说法正确的是
| A.分散系中分散质粒子的大小:Fe (OH)3悬浊液<Fe (OH)3胶体<FeCl3溶液 |
B.可利用反应2CO=2C+O2(此反应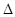 H>O、 H>O、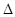 S<0)来消除CO污染 S<0)来消除CO污染 |
| C.若弱酸HA的酸性强于弱酸HB,则相同物质的量浓度的钠盐溶液的碱性:NaA<NaB |
| D.除去Cu粉中混有的CuO,可加入稀硝酸中,充分反应后过滤、洗涤、干燥 |