在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强可使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
某无色溶液,仅由Na+、Ag+、Ba2+、Al3+、AlO2─、MnO4─、CO32─、SO42─中的若干种组成。取该溶液进行如下实验:⑴取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液;⑵在⑴所得溶液中加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;⑶在⑵所得溶液中加入过量Ba(OH)2溶液也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定存在的有
| A.SO42-、AlO2─、Na+、CO32─ | B.CO32─、Na+、Al3+ |
| C.Na+、CO32─、AlO2─ | D.MnO4─、Na+、CO32─ |
常温常压下,在四支试管中分别装入等物质的量混合的两种气体并倒立于水槽中a、NO2、O2 ;b、Cl2、SO2;c、NO、O2;d、NH3、N2,最后水面上升的高度正确的是
| A.b < c< a <d | B.d < a < c<b | C.d < b <a < c | D.d < c <a < b |
已知合成氨的反应为:N2(g)+3H2(g)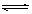 2NH3(g);△H=-QkJ·mo(Q>0)。
2NH3(g);△H=-QkJ·mo(Q>0)。
在同温同压下向密闭容器甲中通入lmolN2和3molH2,达平衡时,放出的热量为QlkJ;
向另一容积相同的密闭容器乙中通入0.5molN2和1.5 molH2,反应达平衡时,放出的热量为Q2kJ。则下列关系式正确的是
| A.2Q2<Ql<Q | B.2Q2=Q1<Q | C.2Q2=Q1=Q | D.Ql<Q2<Q |
目前,科学家正在研究开发一种高能电池——钠硫电池,它以熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na+xS Na2Sx,下列说法中正确的是
Na2Sx,下列说法中正确的是
| A.放电时Na作正极,S极发生还原反应 |
| B.充电时,钠极与外电源的正极相连 |
| C.充电时阳极反应为:xS2--2e-=xS |
| D.若放电时转移0.2 mol 电子,则用去的钠为4.6g |
X+、Y+、M2+、N2-均为含若干电子的短周期元素的简单离子,离子半径大小关系为:N2->Y+、Y+> X+、Y+>M2+、M2+> X+下列比较中正确的是()
| A.原子半径:N可能比Y大,也可能比Y小 |
| B.M2+、N2-核外电子数:可能相等,也可能不相等 |
| C.原子序数:N>M>X>Y |
| D.碱性:M(OH)2>YOH |