下列事实中不能用勒夏特列原理加以解释的是
| A.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.夏天,打开啤酒瓶时会在瓶口逸出气体 |
| D.将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅 |
已知A、B为单质,C为化合物。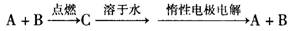
能实现上述转化关系的是
①若C溶于水后得到强碱溶液,则A可能是Na
②若C的溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.②④ C.①③ D.③④
下列离子方程式正确的是
| A.金属钠与水反应:Na+ 2H2O = Na++ 2OH-+ H2↑ |
| B.Ag2S沉淀电离方程式:Ag2S = 2Ag+ + S2- |
| C.Fe3O4与稀硝酸溶液反应: Fe3O4 +8H+ =2Fe3++ Fe2+ +4H2O |
| D.NaHCO3溶液与足量Ba(OH)2溶液混合:2HCO3-+Ba2++2OH- = BaCO3↓+2H2O+CO32- |
下图所示的实验方法、装置或操作完全正确的是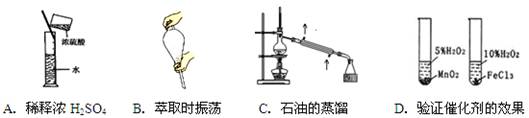
下列叙述正确的是
| A.环丙烷是饱和烃,不能使酸性高锰酸钾溶液褪色 |
| B.乙醇可直接被酸性重铬酸钾溶液氧化 |
| C.氧元素是宇宙中最丰富的元素 |
| D.金属Mg只能用电解法制取 |
将4 mol A气体和2 mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)  2C(g)若经2s 后测得C的浓度为0.6mol·L-1现有下列几种说法:
2C(g)若经2s 后测得C的浓度为0.6mol·L-1现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1
②用物质B 表示的反应的平均速率为0.6 mol·L-1·s-1
③ 2s时物质A的转化率为70%
④ 2s时物质B的浓度为0.7 mol·L-1其中正确的是
| A.①③ | B.①④ | C.②③ | D.③④ |