下列说法中,正确的是
| A.为加快过滤速度,可用玻璃棒在过滤器中搅拌 |
| B.胶体、溶液、浊液分属不同类别的本质是其透过滤纸的性质不同 |
| C.分液漏斗和容量瓶使用前都需要检查是否漏液 |
| D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
下列有关说法正确的是
| A.准确称取0.4000 g NaOH固体可配成100 mL 0.1000 mol·L-1的NaOH标准溶液 |
| B.催化剂可以加快化学反应速率但不能改变化学反应的焓变 |
| C.100 mL pH=3的HA和HB分别与足量的锌反应,HB放出的氢气多,说明HB酸性比HA弱 |
D.对于反应2SO2(g)+O2(g)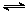 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 |
短周期元素X、Y、Z、W 的原子序数依次增大,X原子的最外层电子数是内层电子数的2倍,X与Z同主族,Y和氢元素同主族,W原子的最外层电子数比次外层电子数少1。下列说法正确的是
| A.元素X形成的单质一定是原子晶体 |
| B.原子半径的大小顺序:r(W)>r(Z)>r(Y) >r (X) |
| C.Y与氧元素形成的化合物Y2O2中阴、阳离子的个数比为1:2 |
| D.W分别与Y、Z形成的化合物中含有的化学键类型相同 |
电浮选凝聚法处理污水的原理如图所示。电解过程生成的胶体能使污水中的悬浮物凝聚成团而除去,电解时阳极也会产生少量气体。下列说法正确的是
| A.可以用铝片或铜片代替铁片 |
| B.阳极产生的气体可能是O2 |
| C.电解过程中H+向阳极移动 |
| D.若污水导电能力较弱,可加入足量硫酸 |
下列表示对应化学反应的离子方程式正确的是
| A.向酸性KMnO4溶液中通入SO2:3SO2+2MnO4-+4OH-=2MnO2↓+3SO42-+2H2O |
| B.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| C.向FeBr2溶液中通入足量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
| D.向新制Cu(OH)2中加入乙醛溶液并加热: |
CH3CHO+2Cu(OH)2+OH- CH3COO-+Cu2O↓+3H2O
CH3COO-+Cu2O↓+3H2O
设NA为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol羟基( )中含有的电子数为0.7 NA )中含有的电子数为0.7 NA |
| B.1 L 0.1 mol·L-1的AlCl3溶液中含有Al3+的数目为0.1 NA |
| C.0.1 mol N2与足量H2反应,转移的电子数为0.6 NA |
| D.标准状况下,1.12 L HCHO中C原子的数目为0.05 NA |