某结晶水合物,含有两种阳离子和一种阴离子,其中所含元素均为短周期元素。为确定其组成,有同学进行了如下实验:称取9.06 g样品,溶于水,将溶液分成两等份,待用。
①向一份溶液中逐滴加入6 mol·L-1 NaOH溶液,先观察到有白色沉淀产生,而后产生使湿润的红色石蕊试纸变蓝色的气体,继续滴加NaOH,白色沉淀又逐渐消失,最后得到无色透明溶液。向其中加入足量BaCl2溶液,可得不溶于稀盐酸的白色沉淀4.66 g。
②取另一份溶液,加入足量6 mol·L-1 NaOH溶液,加热,收集到标准状况下的气体224 mL。然后,往溶液中通入足量CO2,过滤,将所得沉淀洗涤、烘干、灼烧,得白色固体0.51 g。
请回答:
(1)该结晶水合物中含有的两种阳离子是 、 ;一种阴离子是 。
(2)试通过计算确定该结晶水合物的化学式,请写出计算过程。
近年来,工业上用 替代浓
替代浓 作为制取浓
作为制取浓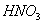 的脱水剂(以下数据均为质量百分比浓度)。65%
的脱水剂(以下数据均为质量百分比浓度)。65%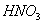 (质量
(质量 )中加72%
)中加72% 溶液(质量为
溶液(质量为 )后蒸馏,分别得到97.5%
)后蒸馏,分别得到97.5%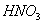 和60%
和60% 溶液(不含
溶液(不含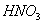 )。
)。
(1)若蒸馏过程中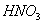 、
、 、
、 均无损耗,求蒸馏前的投料比
均无损耗,求蒸馏前的投料比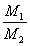 的值。
的值。
(2)蒸馏过程中,若 的损耗占总质量的5.0%,即有
的损耗占总质量的5.0%,即有 的
的 损失,则投料时,比
损失,则投料时,比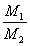 应该_______。(选填增大、减小或不变)
应该_______。(选填增大、减小或不变)
为了配制某培养液,需要用含 和
和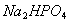 (物质的量比为3∶1)的混合液,每升混合液中含磷元素3.1g。现用4.0mol/L
(物质的量比为3∶1)的混合液,每升混合液中含磷元素3.1g。现用4.0mol/L 液和固体NaOH配制2.0L混合液,问需取该
液和固体NaOH配制2.0L混合液,问需取该 溶液多少毫升?NaOH多少克?
溶液多少毫升?NaOH多少克?
有VL稀硝酸、稀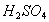 、
、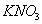 三种物质的混合溶液,已知在该混合液中,
三种物质的混合溶液,已知在该混合液中,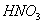 和
和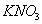 的浓度均为amol/L,而
的浓度均为amol/L,而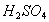 浓度为bmol/L,向该混合液中加入足量的Cu粉,充分反应,放出气体为NO。若反应能进行到底,求出
浓度为bmol/L,向该混合液中加入足量的Cu粉,充分反应,放出气体为NO。若反应能进行到底,求出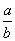 不同的比值范围内,参加反应的Cu的质量。
不同的比值范围内,参加反应的Cu的质量。
在一定温度下,溶质溶解在两种互不相溶的溶剂中的浓度之比是一个常数K,若c(A)、c(B) 分别表示溶质在A、B两种溶剂中的浓度,则有c(A)/c(B)=K。对于
分别表示溶质在A、B两种溶剂中的浓度,则有c(A)/c(B)=K。对于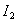 而言,
而言,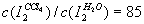 。现有2.0L碘水,其中含
。现有2.0L碘水,其中含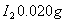 ,若用
,若用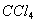 萃取,按两种方法萃取:第一种方法用50mL
萃取,按两种方法萃取:第一种方法用50mL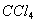 萃取一次;第二种方法是分两次萃取,每次用25mL
萃取一次;第二种方法是分两次萃取,每次用25mL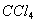 。求两种情况下碘水中残余的
。求两种情况下碘水中残余的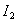 的质量,并指出哪种方法效果好。
的质量,并指出哪种方法效果好。
不同卤素的原子互相可以共用电子对形成一系列化合物,这类化合物叫卤素互化物,现将4.66 g BrCln溶于水,再通入过量SO2,使其发生如下反应:BrCln+(n+1)H2O+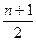 SO2====HBr+nHCl+
SO2====HBr+nHCl+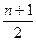 H2SO4
H2SO4
待反应完全后将所得溶液调至中性,再加入过量Ba(NO3)2溶液可生成11.65 g沉淀,试确定BrCln中的n值。