固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2- )在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是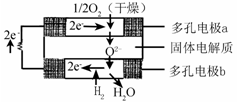
| A.有O2参加反应的a极为电池的负极 |
| B.有H2参加反应的b极为电池的正极 |
| C.a极对应的电极反应式为O2 + 2H2O -4e = 4OH- |
| D.该电池的总反应方程式为:2H2+O2 = 2H2O |
某反应A + B =" C" + D 在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是
| A.△H <0、△S >0 | B.△H >0、△S >0 |
| C.△H <0、△S <0 | D.△H >0、△S <0 |
在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),有关下列图像的说法正确的是
2Z(g),有关下列图像的说法正确的是
| A.依据图a可判断正反应为放热反应 |
| B.在图b中,虚线可表示升高温度 |
| C.若正反应的ΔH<0,图c可表示降低温度使平衡向逆反应方向移动 |
| D.由图d中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0 |
可逆反应:2NO2(g)  2NO(g)+O2(g)在体积固定的密闭容器中进行,能判断达到平衡状态的标志的是
2NO(g)+O2(g)在体积固定的密闭容器中进行,能判断达到平衡状态的标志的是
①单位时间内生成n mol O2的同时生成2n mol NO2
②生成O2的速率等于生成NO2的速率
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②③⑤ | C.①③④⑤ | D.全部 |
已知:强酸和强碱在稀溶液中发生反应时的中和热为57.3 kJ · mol-1,101 k Pa时辛烷的燃烧热为5518 kJ·mol-1。则下列热化学方程式书写正确的是
| A.H++OH-=H2O△H = -57.3kJ·mol-1 |
| B.2NaOH(aq)+ H2SO4(aq)= Na2SO4(aq)+2H2O(l)△H = -114.6 kJ·mol-1 |
| C.2C8H18(l) + 25O2(g) = 16CO2(g)+18H2O(g)△H = -11036 kJ·mol-1 |
| D.2C8H18(l) + 25O2(g) = 16CO2(g)+18H2O(l)△H = -5518kJ·mol-1 |
在同温同压下,下列各组热化学方程式中,△H2>△H1的是
| A.2H2(g)+O2(g)=2H2O(g) △H1;2H2(g)+O2(g)=2H2O(l)△H2 |
| B.S(g)+O2(g)=SO2(g)△H1;S(s)+O2(g)=SO2(g)△H2 |
C.C(s)+ O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g)△H2 O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g)△H2 |
| D.H2(g)+Cl2(g)=2HCl(g)△H1;2H2(g)+2Cl2(g)=4HCl(g)△H2 |