将9.58 g Na2CO3·10H2O与NaHCO3的混合物溶于水配成100mL溶液,测得c(Na+)="1" mol/L,再取同质量的混合物,充分加热至质量不变时,所得固体的质量为
| A.5.30g | B.7.78g | C.6.72g | D.6g |
对于相同体积的K2CO3溶液(浓度为c1)和(NH4)2CO3溶液(浓度为c2),若其中CO32-的物质的量浓度相同,则它们物谢谢质的量浓度c1和c2的关系是()
| A.c1<c2 | B.c1>c2 | C.c1=c2 | D.c1=2c2 |
在密闭容器中进行X2(g)+4Y2(g)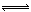 2Z2(g)+3Q2(g)的反应,其中X2、Y2、Z2、Q2的起始浓度分别是0.1mol·L-1、0.4mol·L-1、0.2mol·L-1、0.3mol·L-1当反应达到平衡后,各物质的物质的量浓度不可能是()
2Z2(g)+3Q2(g)的反应,其中X2、Y2、Z2、Q2的起始浓度分别是0.1mol·L-1、0.4mol·L-1、0.2mol·L-1、0.3mol·L-1当反应达到平衡后,各物质的物质的量浓度不可能是()
| A.c(X2)="0.15" mol·L-1 | B.c(Y2)="0.9" mol·L-1 |
| C.c(Z2)="0.3" mol·L-1 | D.c(Q2)="0.5" mol·L-1 |
已知苯酚钠溶液中通入CO2,充分反应后只能生成苯酚和碳酸氢钠;而偏铝酸钠溶液中通入CO2时,可生成氢氧化铝和碳酸钠,则下列说法正确的是()
| A.酸性:苯酚<氢氧化铝<碳酸 |
B.结合氢离子的能力:HCO3-< 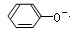 <CO <CO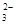 <AlO2- <AlO2- |
| C.同温、同浓度下溶液碱性强弱:偏铝酸钠>碳酸钠>苯酚钠>碳酸氢钠 |
| D.相同条件下,溶液的pH:碳酸氢钠>苯酚钠>碳酸钠>偏铝酸钠 |
类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要通过实验的验证才能决定其正确与否。下列几种类推的结论中正确的是()
| A.已知Fe与S能直接化合得FeS,推测Cu与S化合直接化合生成CuS |
| B.已知A12S3不能在水溶液中存在,推测Mg3N2不能在水溶液中存在 |
| C.已知H2O比H2S的沸点高,推测H2S比H2Se的沸点高 |
| D.已知工业上用电解熔化的NaCl制取Na,推测用熔化的A1C13制取Al |
国际化学组织已将周期表中原主、副族的族号去掉而改称列,如碱金属为第1列,稀有气体为第18列.按此规定属于第13列的元素有()
| A.铜、银、金 | B.氮、磷、砷 | C.硼、铝、镓 | D.锌、镉、汞 |