下列有关阿伏伽德罗定律的说法不正确的是
| A.同温同压下,相同质量的NO和C2H4(气体)体积相同 |
| B.同温同压下,气体的密度之比等于摩尔质量之比 |
| C.同温同压下,相同体积的H2和CO2的原子数之比为2:3 |
| D.同温同体积的气体,若物质的量相同则压强相同 |
下列有关羟基(-OH)与氢氧根(OH-)的说法不正确的是
| A.-OH是不显电性的自由基,OH-是显电性的阴离子 |
| B.二者均可以独立存在 |
C.二者电子式分别为是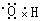 和 和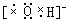 |
| D.-OH不稳定,有极大的活性,OH-很稳定 |
下列化合物中既能使溴的四氯化炭溶液褪色,又能在光照下与溴发生取代反应的是
| A.甲苯 | B.丙烯 | C.乙烯 | D.乙醇 |
3 - 甲基戊烷的一氯代产物有(不考虑立体异构)
| A.6种 | B.5种 | C.4种 | D.3种 |
某种解热镇痛药的结构简式为:当它完全水解时可得到的产物有
| A.5种 | B.4种 | C.3种 | D.2种 |
新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式为:
下列说法正确的是
| A.上述反应为取代反应 | B.上述反应为还原反应 |
| C.滴定时应剧烈振荡锥形瓶 | D.脱氢维生素C的分子式为C6H6O6 |