取100 mL 0.3 mol/L和300 mL 0.25 mol/L的硫酸注入500 mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是
| A.0.21 mol/L | B.0.42 mol/L | C.0.56 mol/L | D.0.26 mol/L |
下列反应的离子方程式,正确的是()
A.Fe2O3溶于过量的氢酸碘中:Fe2O3+6H ====2Fe ====2Fe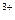 +3H2O +3H2O |
B.向NaAlO2溶液中通人过量CO2:AlO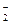 +CO2+2H2O====A1(OH)3↓+CO +CO2+2H2O====A1(OH)3↓+CO |
C.向漂白粉溶液中通人SO2气体:Ca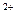 +2C1O +2C1O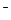 +SO2+H2O====CaSO3↓+2HClO +SO2+H2O====CaSO3↓+2HClO |
D.向Fe(NO3)2溶液中加人稀盐酸:3Fe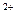 +4H +4H +NO +NO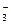 ====3Fe ====3Fe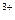 +NO↑+2H2O +NO↑+2H2O |
设阿伏加德罗常数为NA,下列说法正确的是()
| A.用100ml 4mol/L盐酸与8.7gMnO2共热能制取氯气0.2NA |
| B.一定温度下0.1L 0.1mol/L的HA和1L0.01mol/L的HA所含A-微粒数均为0.01NA |
| C.4.5 gSiO2晶体中含有的硅氧键数目为0.3 NA |
| D.用Pt做电极电解硝酸铜溶液,当阳极产生的气体在标况下为22.4L,转移电子数目为NA |
下列变化中涉及化学变化的是()
⑴爆竹燃放⑵碘的升华⑶金属钝化⑷铝热反应⑸干冰汽化⑹加热氯化铵⑺甘油加水作护肤剂⑻明矾净水⑼蜂蚁螫咬后涂稀氨水可以减痛⑽医用酒精可用于皮肤消毒⑾烹鱼时加入少量的料酒和食醋可减少腥味⑿橡胶老化⒀用四氯化碳可擦去圆珠笔油渍⒁蛋白质的盐析
| A.⑴⑶⑷⑸⑺⑿⒀ | B.⑵⑷⑸⑺⑿⒀⒁ |
| C.⑵⑸⑺⒀⒁ | D.以上选项均不正确 |
温度为T0时,在容积固定的密闭容器中发生反应,各物质的浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示。下列叙述正确的是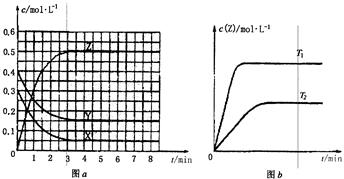
| A.该反应的正反应是放热反应 |
| B.起始时若X、Y的浓度变为原来的2倍,建立的平衡状态与原平衡不等效 |
| C.图a中反应达到平衡时,Y的转化率为37.5% |
D.反应时各物质的反应速率关系为: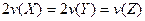 |
下列有关溶液的说法中,正确的是
| A.相同物质的量浓度的下列溶液中:①NH4Al(SO4)2②NH4Cl③CH3COONH4④NH3·H2O,c(NH4+) 由大到小的顺序是:①>②>③>④ |
B.物质的量浓度相等的 H2S 和 NaHS 混合溶液中:c(Na +) + c(H+) = c(S2―) + c(HS―) + c(OH―) +) + c(H+) = c(S2―) + c(HS―) + c(OH―) |
| C.同温时,HF比HCN易电离,则NaF溶液的pH 比NaCN 溶液的pH小 |
| D.常温下,BaSO4(s)在纯水中的溶解度与在稀硫酸溶液中溶解度相同 |