设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.一定条件下,0.2molSO2与足量O2充分反应,生成SO3分子数为0.2NA |
| B.常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA |
| C.标准状况下,2.24LCl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |
| D.标准状况下,22.4L甲苯中含C—H数目为8NA |
一定温度下,满足下列条件的溶液一定呈酸性的是
A.pH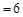 的某物质的水溶液 的某物质的水溶液 |
B.加酚酞后显无色的溶液 |
| C.能与金属Al反应放出H2的溶液 | D.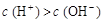 的任意物质的水溶液 的任意物质的水溶液 |
下列叙述中,正确的是
| A.只含有金属元素的离子不一定是阳离子 |
| B.金属阳离子被还原不一定得到金属单质 |
| C.氧化还原反应中,非金属单质必是氧化剂 |
| D.元素从化合态变为游离态时,一定被还原 |
重水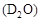 是重要的核工业原料,下列关于D原子的说法错误的是
是重要的核工业原料,下列关于D原子的说法错误的是
A.氘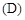 原子核外有1个电子 原子核外有1个电子 |
B.是H的同位素 |
| C.自然界中没有D原子存在 | D.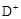 质量数为2 质量数为2 |
下列物质不能通过置换反应得到的是
| A.CO | B.F2 | C.C | D.Fe3O4 |
化学与社会、生产、生活密切相关。下列做法值得提倡的是
| A.SO2作为食品漂白剂 | B.氟里昂作为制冷剂 |
| C.Na2CO3治疗胃酸过多 | D.“地沟油”制取肥皂 |