燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)污染也跟冬季燃煤密切相关。SO2、CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)光气 (COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)
 COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中固定体积容器内各物质的浓度随时间变化的曲线。回答下列问题:
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中固定体积容器内各物质的浓度随时间变化的曲线。回答下列问题:

① 0~6 min内,反应的平均速率v(Cl2)= ;
②下列说法不能判断该反应达到化学平衡状态的是 。(填字母)
| A.体系中Cl2的转化率不变 |
| B.体系中气体的平均摩尔质量不再改变 |
| C.每消耗1mol CO的同时生成1mol COCl2 |
| D.混合气体密度不变 |
③随温度升高,该反应平衡常数变化的趋势是 ;(填“增大”、“减小”或“不变”)
④比较第8 min反应温度T(8)与第15 min反应温度T(15)的高低:T(8) T(15)
(填“<”、“>”或“=”)。
⑤若保持温度不变,在第7 min 向体系中加入这三种物质各2 mol,则平衡
移动(填“向正反应方向”、“向逆反应方向”或“不”);
(2)有一种用CO2生产甲醇燃料的方法:CO2+3H2 CH3OH+H2O
CH3OH+H2O
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-b kJ·mol-1;
H2O(g)=H2O(l)△H=-c kJ·mol-1;
CH3OH(g)=CH3OH(l)△H=-d kJ·mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:____________________________;
(3)如图所示,利用电化学原理将SO2转化为重要化工原料C

若A为SO2,B为O2,则负极的电极反应式为:________________________;
铁及其化合物在生产、生活中有着广泛的应用。
(1)下图是研究海水对铁闸不同部位腐蚀情况的剖面示意图。
在图中A、B、C、D四个部位中,生成铁锈最多的部位________(填字母)。
(2)已知t℃时,反应FeO(s)+CO(g)  Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=____________;t℃时,反应达到平衡时n(CO):n(CO2) =_______;t℃时,若在1L密闭容器中加入0.02 mol FeO(s)、xmol CO,发生反应,当反应达到平衡时FeO(s)的转化率为50%,则x=________。
Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=____________;t℃时,反应达到平衡时n(CO):n(CO2) =_______;t℃时,若在1L密闭容器中加入0.02 mol FeO(s)、xmol CO,发生反应,当反应达到平衡时FeO(s)的转化率为50%,则x=________。
(3)高铁酸钾是一种高效、多功能的水处理剂。工业上常采用NaClO氧化法生产,有关
反应原理为:
3NaClO+2Fe(NO3)3+l0NaOH=2Na2FeO4 ↓+3NaCl+6NaNO3+5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
实验证明,反应的温度、原料的浓度及配比对高铁酸钾的产率都有影响。图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图2为一定温度下,NaClO不同质量浓度对K2FeO4生成率的影响。
①工业生产中,反应进行的适宜温度为_________℃;此时Fe(NO3)3与NaClO两种溶液的理想的质量浓度之比是____________。
②高铁酸钾做水处理剂时的作用主要有__________________(答出2条即可)。
下表是元素周期表的一部分,表中每一序号分别代表一种元素。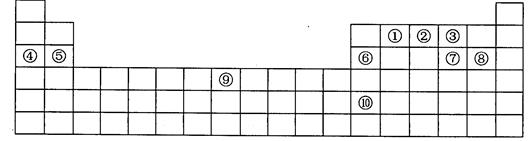
(1)元素⑥的元素名称是_______。元素⑤位于元素周期表________区。
(2)元素①原子的价电子数是________。元素⑨在元素周期表的第4周期第_______族。
(3)在元素①、②、③中,非金属性最强的是________(用所对应的元素符号表示。下同)元素③、⑦、⑧的简单离子的半径由大到小的顺序为______________。
(4)元素性质周期性变化的实质是元素原子______________的周期性变化。元素⑩的单质可能具有的性质是___________(填字母)。
a.能导电导热
b.能与稀盐酸反应生成氢气
c.其晶体属离子晶体
(5)在元素④、⑤、⑥的最高价氧化物中,具有两性的是__________(填化学式)。在元素①~⑩的最高价氧化物的水化物中,酸性最强的是___________(填化学式)。
(6)元素⑨原子的外围电子排布为________________。
A、B、C、D、E为短周期元素,A~E原子序数依次增大,质子数之和为40,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E是地壳中含量最多的金属元素。试回答:
(1)B元素在周期表中的位置为____________;
(2)将D的单质投入A2C中,反应后得到一种无色溶液。E的单质在该无色溶液中反应的离子方程式为___________。
(3)经测定,A2C2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式__________。过去常用硫酸处理BaO2来制备A2C2,写出该反应的离子方程式_______________;
现在实验室可以将过氧化钠加入到水中来制取A2C2,写出该反应的化学方程式__________________;
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到了上述目的,又保护了环境,试写出反应的离子方程式___________。
(5)元素D的单质在一定条件下,能与A单质化合生成一种氢化物DA,熔点为800℃。
①DA能与水反应放氢气,反应化学方程式是。
②若将1mol DA和1 mol E单质混合加入足量的水,生成气体的体积是(标准状况下)L
(1)甲烷(CH4)的摩尔质量为;
(2)8 g CH4中约含有个分子、含有mol电子,在标准状况下所占的体积约为L;
(3)所含原子数相等的甲烷和氨气(NH3)的质量比为。
(1)与明矾相似,硫酸铁也可用作净水剂,其原理为_________(用离子方程式表示)。
(2)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为___________________。
(3)已知:S2O32—有较强的还原性,实验室可用I-测定K2S2O8样品的纯度,反应方程式为S2O82—+2I-=2SO42—+I2①、I2+2S2O32-=2I-+S4O62—②。S2O82—、S4O62—、I2氧化性强弱顺序:__________。
(4)已知溶液中,还原性为HSO3—>I-,氧化性为IO3—>I2>SO42—。在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
a点处的还原产物是__________(填离子符号);
b点→c点反应的离子方程式是__________________。