Zn(OH)2是两性氢氧化物,和强酸反应时生成Zn2+,跟强碱反应时生成ZnO22-.现有三份等物质的量浓度、等体积的MgCl2、ZnCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液,分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如下图所示,则与MgCl2、ZnCl2、AlCl3三种溶液一一对应的正确图象是
| A.③②① | B.③②④ | C.③⑤① | D.③⑤④ |
下列物质中,氮元素的化合价最低的是
| A.N2 | B.NH3 | C.NO | D.NO2 |
水是一种非常宝贵的资源,保护水资源已逐步成为人们的一种共识。下列行为不会造成水体污染的是
| A.含重金属离子的废水大量排放 | B.含磷洗衣粉的大量使用 |
| C.生活污水的任意排放 | D.利用太阳能将海水淡化 |
下列反应中,属于氧化还原反应的是
| A.2Na2O2 + 2CO2= 2Na2CO3+ O2 |
| B.Na2O + CO2= Na2CO3 |
| C.2NaOH + CO2 = Na2CO3+ H2O |
| D.CaCO3 =" CaO+" CO2↑ |
下列离子方程式书写正确的是
| A.钠和冷水反应: Na+2H2O=Na++2OH—+H2↑ |
| B.铁粉投入到硫酸铜溶液中:Fe+Cu2+ =Fe2++Cu |
| C.AlCl3溶液中加入足量的氨水:Al3++ 3OH=Al(OH)3↓ |
| D.澄清石灰水跟稀硝酸反应: Ca(OH)2+2H+ =Ca2++2H2O |
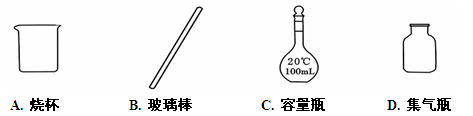
配制100mL2.0mol·L-1Na0H溶液时,不需要用到的仪器是