下列离子方程式中书写正确的是
| A.氯化铝溶液中加入足量的氨水:Al3++3NH3·H2O= Al(OH)3 ↓+3NH4+ |
| B.水玻璃中加入稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ |
| C.二氧化硅与苛性钠溶液反应:SiO2+OH-=SiO32-+H2O |
| D.氧化铝与NaOH溶液反应:Al2O3+10OH-= 2[Al(OH)4]-+H2↑ |
一定条件下,尿素[CO(NH2)2]与NO反应生成N2和另 外2种对环境无污染的氧化物。如图是 CO(NH2)2与某种烟气中NO的物质的量之比分别为1:2、2:1、3:1时,NO脱除率随温度(t)变化的图像。下列说法错误的是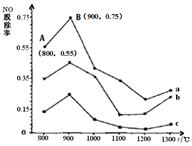
| A.尿素脱除NO的反应为:2CO(NH2)2 + 6NO=2CO2 + 4H2O + 5N2 |
| B.图中a,对应CO(NH2)2与NO的物质的量之比为1:2 |
| C.在900℃左右,NO的脱除率最佳 |
| D.NO的起始浓度为6×10-4 mg / m3,图中a从A点到 B点经过0.8 s,这段时间内NO的脱除平均速率为1.5×10-4 mg / (m3·s) |
如图,石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质。图示装置工作时,生成的金属钙能还原二氧化钛制备金属钛。下列说法不正确的是
| A.阳极反应式为C + 2O2- - 4e-=CO2↑ |
| B.由TiO2制得1mol 金属Ti ,理论上外电路转移4 mol电子 |
| C.制备金属钛前后,装置中CaO的量不变 |
| D.TiO2在阴极放电 |
A、B、C均为中学常见的单质或化合物,一定条件下,存在转化关系:A + H2O → B + C 。下列说法正确的是
A.若B为强碱,则A一定为金属钠 B.若B为强酸,则A一定为氯气
C.若C为H2,则H2O一定作氧化剂 D.若C为O2,则H2O一定作还原剂
能达到实验目的的是
| A.称NaOH固体的质量 | B.读数为10.60 | C.反应热的测定 | D.收集氯气 |
下列说法正确的是
| A.有化学键断裂的过程一定发生化学变化 |
| B.氯化钠是一种电解质,电解饱和食盐水可制得金属钠 |
| C.将pH=a的醋酸稀释为pH=a + 1的过程中,c(CH3COOH) / c(H+)减小 |
| D.SiO2是酸性氧化物,能与强碱溶液反应,但不与任何酸反应 |