硫铁矿烧渣是一种重要的化工生产中间产物,主要成分是Fe3O4、Fe2O3、FeO和SiO2等。下面是以硫铁矿烧渣制备高效净水剂聚合硫酸铁的流程图:
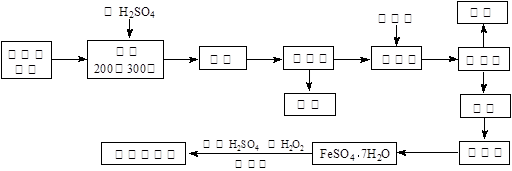
(1)实验室实现“操作I”所用的玻璃仪器有玻璃棒、 和烧杯;
(2)硫铁矿烧渣在“酸溶”前要粉碎的主要目的是 ,检验“酸溶”后的溶液中含有Fe2+的试剂及现象是 ;
(3)“操作Ⅲ”系列操作名称依次为 、冷却结晶、过滤和洗涤。洗涤沉淀的方法是 ;
(4)加入适量H2O2的目的是氧化Fe2+,写出H2O2氧化Fe2+为Fe3+的离子方程式: 。
用化学符号填空
氮元素 两个氢离子 氧分子
五氧化二磷中磷元素的化合价
已知某粗盐样品含有Na2SO4、MgCl2、CaCl2等杂质。实验室提纯流程如下: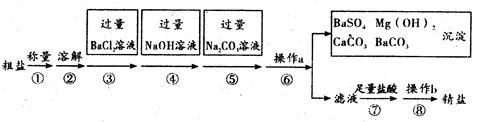
(1)操作a的名称为 ,在操作b中玻璃棒的作用是 。
(2)进行步骤③后,判断BaCl2过量的方法是 (写出步骤、现象)。
(3)步骤⑤的目的是 ,步骤⑦中能用稀硫酸代替稀盐酸吗? 。
根据所给仪器,回答下列回问题
(1)配置100g5%的氯化钠溶液,需要胶头滴管、药匙、托盘天平和上述仪器中的(填序号) ,量取液体时,由于读数时仰视造成所配溶液的溶质质量分数 (填“偏大”、“偏小”或“不变”)。
(2)在实验室,某同学要利用所给仪器制取一瓶氧气,应选用的仪器有(填序号) ,反应的化学方程式为 。若用如图所示的装置来收集该气体,气体应从 (填“a”或“b”)通入。
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“—”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质)。回答下列问题
(1)A的化学式为 ,D→C的化学方程式为 ;
(2)若E和F均由两种元素组成,E的化学式为 ;
(3)若E和F均由三种元素组成,写出指定的转化反应的化学方程式:F→B+C 。
结构决定物质的性质、变化,请结合下图回答问题。
(1)由图1可知,在常温下,碳的化学性质不活泼的微观原因是 ;
(2)图2中A的化学式可能是 ,写出与图2反应微观本质不同的一个化学方程式 。