在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品。用图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A是利用盐酸和石灰石制取CO2的装置,A中发生反应的化学方程式为_____________.
(2)填写表中空格:
| 仪器 |
加入试剂 |
加入该试剂的目的 |
| B |
饱和NaHCO3溶液 |
|
| C |
|
|
| D |
|
|
(3)写出过氧化钠与二氧化碳反应的化学方程式:__________________。
在此反应中,过氧化钠的作用是_______(填序号) ①氧化剂;②还原剂;③既是氧化剂又是还原剂;④既不是氧化剂,又不是还原剂。
(4)试管F中收集满气体后,下一步实验操作是:___________________________。
(12分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为:
2NH3+3CuO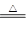 N2+3H2O+3Cu,用示意图中的装置可以实现该反应,A中加的是氯化铵和氢氧化钙固体,C中的固体是氧化铜。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应,A中加的是氯化铵和氢氧化钙固体,C中的固体是氧化铜。回答下列问题: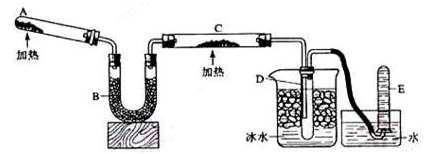
(1)A中制备氨气的反应方程式为。
(2)B中加入的物质是。(填名称)
(3)实验时C中观察到的现象是 。
(4)实验时在D中收集到的液态物质是。(填名称)
(5)已知反应前C中固体的质量为m1g,反应一段时间后停止反应,冷却至室温测量C中固体的质量为m2g,则理论上E中最多收集到的气体体积为(换算成标准状况下的体积)(用m1、m2表示)。
(13分)工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下: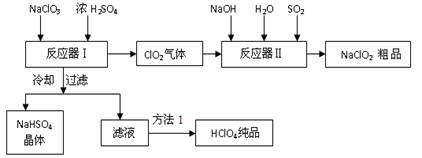
已知:
1.NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
2.高氯酸是至今为止人们已知酸中的最强酸,沸点90℃。
请回答下列问题:
(1)反应器Ⅰ中冷却的目的是,方法1使用的操作是。
(2)反应器Ⅱ中发生反应的离子方程式为 。
(3)通入反应器Ⅱ中的SO2用另一物质H2O2代替同样能生成 NaClO2,请简要说明双氧水在反应中能代替SO2的原因是。
(4)Ca(ClO)2、ClO2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有,请写出工业上用氯气和NaOH溶液生产另一种消毒剂 NaClO的离子方程式。
浓H2SO4与炭反应,产物成分可用下图装置来确认: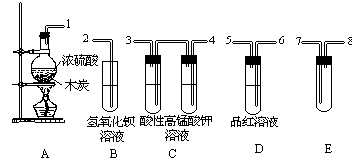
(1)A 装置中反应的化学方程式为;
(2)B 装置中反应的离子方程式;
(3)装置 C 的作用是,E中盛放的试剂是_______;
(4)请用1、2…等标号,写出装置的连接顺序:1-。
已知苯甲酸微溶于水,易溶于乙醇、乙醚,有弱酸性,酸性比醋酸强。它可用于制备苯甲酸乙酯和苯甲酸铜。
(一)制备苯甲酸乙酯
相关物质的部分物理性质如表格:
实验流程如下:
(1)制备苯甲酸乙酯,下列装置最合适的是,反应液中的环己烷在本实验中的作用。
(2)步骤②控制温度在65~70℃缓慢加热液体回流,分水器中逐渐出现上、下两层液体,直到反应完成,停止加热。放出分水器中的下层液体后,继续加热,蒸出多余的乙醇和环己烷。反应完成的标志是_______。
(3)步骤③碳酸钠的作用是,碳酸钠固体需搅拌下分批加入的原因。
(4)步骤④将中和后的液体转入分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水MgSO4干燥。乙醚的作用。
(5)步骤⑤蒸馏操作中,下列装置最好的是________(填标号),蒸馏时先低温蒸出乙醚,蒸馏乙醚时最好采用(水浴加热、直接加热、油浴加热)。
(二)制备苯甲酸铜
将苯甲酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2粉未,然后水浴加热,于70~80℃下保温2~3小时;趁热过滤,滤液蒸发冷却,析出苯甲酸铜晶体,过滤、洗涤、干燥得到成品。
(6)混合溶剂中乙醇的作用是_______________,趁热过滤的原因________________
(7)本实验中下列药品不能代替氢氧化铜使用的是_____________________
A.醋酸铜B.氧化铜 C.碱式碳酸铜 D.硫酸铜
(8)洗涤苯甲酸铜晶体时,下列洗涤剂最合适的是________
A.冷水 B.热水C.乙醇 D.乙醇水混合溶液
某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验.
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:
(1)实验时,过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为.
(2)检验沉淀B已洗净操作是.
(3)在整个实验过程中托盘天平至少使用次.
(4)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为____________.
方案Ⅱ.乙组同学的主要实验按如下图所示装置进行实验:

(5)该实验中装置B盛放的物质是__________,分液漏斗中(填“能”或“不能”)用盐酸代替稀硫酸进行实验.
(6)在C中装碱石灰来吸收净化后的气体.
①样品中碳酸钠的质量分数越大,则实验中吸收净化后气体的干燥管在充分吸收气体前后的质量差____________________(填“越大”、“越小”或“不变化”)
②D装置的作用是_________________.
(7)有的同学认为为了减少实验误差,在反应前后都要通入N2(如图),反应后通入N2的目的是_____________________.