(1)下列物质的微观示意图中,表示混合物的是 (填序号,下同),表示氧化物的是 ,属于单质的是_____________。

(2)书写化学方程式时出现的错误类型包括:A.反应物或生成物化学式书写错误 B.未配平
C.遗漏反应条件 D.遗漏“↑”或“↓”。判断下列化学方程式的错误类型(填序号)。
| 序号 |
化学方程式 |
错误类型 |
| ① |
P + O2点燃 P2O5 |
|
| ② |
H2O +CO2 H2CO2 |
|
| ③ |
2H2O 通电 2H2↑+ O2 |
|
| ④ |
2CO+2O2 2CO2 |
|
(3)①地壳中含量最多的元素是 ;②温度计中填充的液态金属是 ;
③水中氧元素的化合价 ;④Fe2+ 中2的含义 ;⑤CO2中2的含义 。
(4)除去二氧化碳中混有的少量一氧化碳可用( );除去一氧化碳中混有的二氧化碳可用( );除去氧化铜混有的中少量碳粉可用( )
A.澄清石灰水 B.灼热氧化铜 C.点燃的方法
D.在密闭容器中加强热 E.在氧气流中灼烧
人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。下图是金属在实际生活中的应用。


电线金属丝炊具
(1)地壳中含量最高的金属元素是。
(2)根据上图推断,说出金属具有的两点物理性质有____________ 、____________。
(3)2008年奥运会主运动场“鸟巢”使用了大量的钢铁。钢铁与直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈。
(4)用稀硫酸除去铁锈,其反应的化学方程式是。
某农场附近新建了一座燃煤火力发电厂后该农场的小麦产量急剧下降。经农场技术员测定:雨水pH约为4、土壤pH约为5。已知一些重要作物最适宜生长的土壤的pH如下表: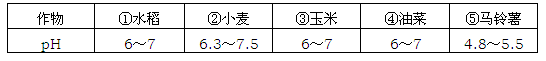
(1)据上表数据,你认为这种土壤最适合种植的作物是(填编号)_________。
(2)继续种小麦,你认为最好选用以下(填编号)________试剂来改良土壤。
①工业盐酸②熟石灰③纯碱
(3)该地区形成酸雨的主要原因是。
在我们的生活中,许多现象与化学有着密切的联系,从下列物质中选择恰当物质填空:小苏打、硫酸、熟石灰、活性炭、一氧化碳、甲醛、烧碱、氯化钠
生理盐水是医疗上常用的溶液,该溶液的溶质是_________;发酵粉可以使食品松软可口,属于发酵粉成分之一的是;农业技术人员对某些菜地的土壤进行分析,发现土壤呈酸性,不利于作物生长。你认为应当施用适量的___________来改良土壤结构;用于除去冰箱异味的是_________;用于制作动物标本的是________;用煤炉取暖时易发生中毒,主要是由于室内______排放不畅而引起的。
5月20日是“中国学生营养日”,请你用所学化学知识关注营养问题:
(1)妈妈每天为小东准备的食品有:奶类、豆类、鱼肉类、水果、蔬菜、面食等,这些食品中含有______________、_____________等人体所需营养素(只需填写两种即可),可以保证营养均衡。
(2)同学们喜爱喝的酸奶,其配料表部分为:①纯净水②鲜牛奶③白砂糖④柠檬酸⑤食用香精⑥维生素E等多种维生素。其中能为人体提供能量的是(填编号)。
们日常生活与化学密切相关.
(1)汽车燃烧的汽油和做饭燃烧的天然气等均为化石燃料产品.化石燃料属(填“可再生”或“不可再生”)能源.
(2)雨后晴天的空气清新洁净,此时的空气属于(填“纯净物”或“混合物”).
(3)下列着火的应急处理不合理的是(填序号).
①实验室燃着的酒精灯被碰倒着火,立即用湿毛巾盖灭;
②油在炒菜锅内因温度过高着火,立即向锅内倒入冷水灭火;
③电器着火时,立即断电,再用干粉灭火器灭火.