羟基是重要的官能团。某化学小组以下列4种物质的溶液作为研究对象,比较不同物质的羟基中氢原子的活泼性。①碳酸 ②乙醇 ③苯酚 ④乙酸
I.甲同学设计并实施了如下实验方案,请完成(1)(2)(3)(4)的填空及结论。
| 编号 |
实验操作 |
实验现象 |
结论及解释 |
| 1 |
分别取4种溶液,滴加紫色石蕊溶液 |
溶液变红的是①④溶液 |
略 |
| 2 |
向含酚酞的NaOH溶液中,各滴加等量的②③两种溶液 |
②中无明显现象 ③中红色明显变浅 |
滴加③时反应的化学方程式: (1)___________ |
| 3 |
用一定浓度的醋酸溶液浸泡水垢(水垢主要成分为碳酸钙) |
(2)__________ |
略 |
| 4 |
将CO2通入C6H5ONa溶液中 |
(3)__________ |
反应的化学方程式: (4)_____________ |
| 结论: 4种物质的羟基中的氢原子的活泼性由强到弱的顺序是(填序号)_____________。 |
II.乙同学在研究了甲同学的实验方案后,提出如下改进方案,能一次比较乙酸、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如下图所示。

(1)利用上述仪器组装实验装置,其中A管插入(填字母,下同)_______中,B管插入E中,C管插入_________中。
(2)丙同学查资料发现乙酸有挥发性,于是在试管F之前增加了一个盛有_____________溶液的洗气装置,使乙同学的实验设计更加完善。
化学实验是实现科学探究的重要途径。请将下列有关实验的问题填写完整。
(1)下图是探究氯气性质的部分实验装置。实验室可用浓盐酸与二氧化锰共热来制取氯气,同时生成二氯化猛(MnC12)和水,该反应的化学方程式为;实验时,A装置中的KI淀粉试纸变蓝色,其原因是;B装置中可观察到的现象是;C装置中NaOH溶液的作用是,有关反应的离子方程式为。
(2)某研究性学习小组的同学用以下仪器组合的装置制取氨气,并探究氨气与氧化铜反应的性
质(已知:2NH3+3CuO
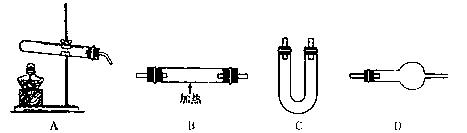
请从上图中选用所需的仪器组成一套装置制取氨气,并使氨气与氧化铜反应,同时证明该反应有水生成。下表是按仪器的连接顺序由上至下依次填写的,请将该表补充填写完整。
| 选用的仪器(填字母) |
加入的试剂 |
作用 |
| 反应器(或发生气体) |
||
| C |
||
| 氧化铜 |
使氨气与氧化铜反应 |
|
某实验小组想验证Mg粉和CO2的反应,请从下图中选用所需的仪器(可重复选用)组成一套进行该实验的装置。现提供浓H2SO4、稀盐酸、镁粉、大理石、澄清石灰水,饱和NaHCO3溶液、饱和Na2CO3溶液。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)。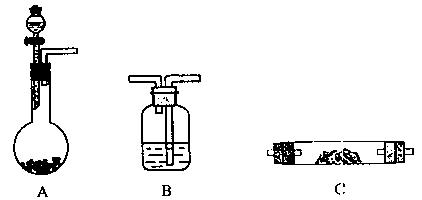
(1)将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加的试剂(可不填满)
| 选用的仪器(填字母) |
加入的试剂 |
| A |
稀盐酸、大理石 |
(2)A中发生反应的离子方程式为。
(3)组装好仪器,检查气密性良好,加入药品。在加热反应管C之前应进行的操作和目的是
。
(4)反应中C装置的主要现象是。
(1)配制 1 mol/L的CuSO4溶液500ml,需胆矾① g;用托盘天平称出,把称好的胆矾放入② 里,用适量蒸馏水使它完全溶解,把制得的溶液小心地转移到③中,用适量蒸馏水洗涤烧杯、玻璃棒2~3次,把每次的洗涤液都注入④ 中,然后慢慢地加入蒸馏水到液面在刻度线下⑤ ,改用⑥ 滴加蒸馏水到刻度,使溶液的⑦ ;把瓶塞盖好,用⑧ 顶住瓶塞,另一只手⑨ ,将瓶底倒转、摇匀。
(2)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不变”)
①定容时俯视容量瓶的刻度线。
②如果加水超过了刻度线,取出水使液面恰好到刻度线。
(8分)氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现有0.001mol/L酸性KMnO4和未知浓度的无色NaHSO3溶液,反应离子方程式是2MnO4- + 5HSO3- + H+ ==2Mn2+ + 5SO42-+ 3H2O填空回答问题:
(1)该滴定实验所需仪器有下列中的______________________________(填序号)
| A.酸式滴定管 | B.碱式滴定管 | C.量筒 | D.锥形瓶E.铁架台F.滴定管夹G.烧杯H.白纸I.胶头滴管J.漏斗 |
(2)滴定前平视KMnO4溶液,刻度为a mL,若滴定后(终点)俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积_________( 多、少)。根据(b-a)mL计算得到的待测液浓度比实际的浓度_________(大、小)。
下列实验中,不能达到预期的目的的是(填选项编号)
| A.用升华法分离碘和苯的混合物 |
| B.用分液法分离水和硝基苯的混合物 |
| C.将甲烷与氯气混合光照制二氯甲烷 |
| D.用电石和饱和食盐水制乙炔 |
E. 用酒精和浓硫酸混合加热至170℃制乙烯