制取新型水处理剂ClO2的化学方程式为:
2KClO3+H2C2O4+H2SO4 2ClO2+K2SO4+2CO2+2H2O。下列说法不正确的是( )
2ClO2+K2SO4+2CO2+2H2O。下列说法不正确的是( )
| A.KClO3在反应中得到电子 | B.ClO2是还原产物 |
| C.H2C2O4 在反应中被氧化 | D.1mol KClO3参加反应有2mol电子转移 |
用于鉴别K2CO3和KHCO3的溶液,最适宜的方法应当是( )
| A.焰色反应 |
| B.滴加Ba(OH)2溶液 |
| C.加入少量盐酸 |
| D.滴加CaCl2稀溶液 |
下列有关焰色反应的实验操作注意事项的说明,其中正确的是( )
①钾的焰色要透过蓝色钴玻璃观察②先将铂丝灼烧到与原火焰颜色相同,再蘸取被检物质③每次实验完,均要用盐酸洗净铂丝④实验时,要尽可能选用本身颜色较浅的火焰
| A.只有① | B.只有③ |
| C.①②③ | D.全部 |
向含有下列各组离子的溶液中滴加NaOH溶液,得到白色沉淀的是( )
| A.Ba2+ HCO- 3K+ Cl- |
B.Na+ CO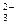 OH- NO OH- NO |
C.Na+ OH- SO CO CO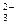 |
| D.Mg2+ NO- 3Na+ Cl- |
下列离子方程式不正确的是( )
| A.碳酸钠溶液和盐酸反应 Na2CO3+2H+  2Na++CO2↑+H2O 2Na++CO2↑+H2O |
| B.过氧化钠和水反应 2Na2O2+2H2O  4Na++4OH-+O2↑ 4Na++4OH-+O2↑ |
| C.钠跟水反应 Na+H2O  Na++OH-+H2↑ Na++OH-+H2↑ |
| D.碳酸氢钠溶液跟稀硝酸反应 |
HCO +H+
+H+ CO2↑+H2O
CO2↑+H2O
下列灭火剂能用于扑灭金属钠着火的是( )
| A.干冰灭火剂 |
| B.黄沙 |
| C.干粉(含NaHCO3)灭火剂 |
| D.泡沫灭火剂 |