【化学——选修2:化学与技术】
工业上以Al(OH)3、H2SO4、(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图所示:

回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为 。
(2)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O NH3·H2O+H+,则该反应的平衡常数为 。
NH3·H2O+H+,则该反应的平衡常数为 。
(3)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为 。
(4)固体NH4Al(SO4)2·12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体的成分为 。

(5)综上分析,流程图中M混合气体的主要成分的化学式为 。M可用一种物质吸收以实现循环利用,该物质的名称是 。
将6g CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为_____,经测定溶液中含CH3COO-为1.4×10-3mol/L,此温度下醋酸的电离常数:Ka=_______,温度升高,Ka将_____。
(6分)用中和滴定的方法测定NaOH和Na2CO3的混合液中NaOH含量时,可先在
混合液中加入过量的BaCl2溶液,使Na2CO3完全变成BaCO3沉淀,然后用标准盐酸滴定(用酚酞做指示剂),试回答:
(1)滴定时BaCO3能否溶解?理由是_____________________________________.
(2)如用甲基橙作指示剂,则测定的结果________(填“偏高”、“偏低”或“无影响”).
(12分)已知95℃时水的离子积Kw=1×10-12,25℃时Kw=1×10-14,回答下列问题:
(1)95℃时水的电离常数________(填“>”“=”或“<”) 25℃时水的电离常数.
(2)95℃纯水中c(H+)________(填“>”、“=”或“<”)c(OH-).
(3)95℃时向纯水中加入NaOH,c(OH-)=1×10-1 mol/L,此时pH=________.
在537℃、101KPa 时,往容积可变的密闭容器中充入2mol SO2、 1mol O2,此时容器的体积为200L。向容器中加入催化剂(固体)并保持恒温恒压,发生反应:2SO2(g)+O2(g) 2SO3(g)达到平衡时,平衡气体中SO3的体积分数为91%。试回答下列问题:
2SO3(g)达到平衡时,平衡气体中SO3的体积分数为91%。试回答下列问题:
(1)保持上述温度和压强不变,若向容器中只充入2mol SO3并加入固体催化剂。则平衡时,SO2的体积分数是,容器的体积为L。
(2)若温度和容器的容积不变,则平衡时的容器内气体的压强为KPa。
(3)温度仍保持537℃,容器体积保持200L不变(恒容)。充入a molSO2、b molO2,并加入固体催化剂,反应达平衡时,SO3的体积分数仍为0.91,体系压强为101KPa。若a:b=2:1,则a=。
在t℃时,将3molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A (g)+B (g) 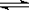 x C(g),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L。据此填写以下空白:
x C(g),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L。据此填写以下空白:
(1)v(B) =mol/(L·min), x的值=。
(2)比较达到平衡时,A、B两反应物的转化率之比为α(A):α(B)=;
(3)若继续向原平衡混合物的容器中通入少量氦气后(氦气和A、B、C都不反应),则下列说法中正确的是____________(填写字母序号)
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动D.气体A的浓度会减小