科学家尝试用微生物电池除去废水中的有害的有机物,其原理如图所示。下列有关说法错误的是
A.A极电极反应式为: |
| B.B极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ |
| C.溶液中的阴离子由A极向B极移动 |
| D.该微生物电池在高温条件下无法正常工作 |
元素周期表中铋元素的数据见右图,下列说法正确的是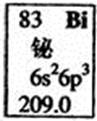
| A.Bi元素的质子数是209 |
| B.Bi元素的相对原子质量是209.0 |
| C.Bi原子6p亚层有一个未成对电子 |
| D.Bi原子最外层有5个能量相同的电子 |
某物质熔融状态可导电,固态可导电,将其投入水中形成的水溶液也可导电,则可推测该物质可能是
| A.金属 | B.非金属 | C.可溶性碱 | D.可溶性盐 |
对于钠原子的第3层电子的p轨道3px、3py、3pz间的差异,下列几种说法中正确的是
| A.电子云形状不同 | B.原子轨道的对称类型不同 |
| C.电子(基态)的能量不同 | D.电子云空间伸展的方向不同 |
下列叙述正确的是
| A.Na、Mg、Al元素最高化合价依次升高 |
| B.P、S、Cl元素最高价氧化物对应的水化物酸性依次增强 |
| C.N、O、F元素非金属性依次减弱 |
| D.Li、Na、K原子的电子层数依次增多 |
从1897年英国首次使用氯气对给水管网消毒以来,氯气用于自来水消毒已经经历了100多年的历史。目前,我国大多数城市仍然采用氯气消毒法对自来水进行净化、消毒。氯气之所以长期用于自来水消毒,原因是
| A.氯气有毒,可以毒死细菌、病毒 |
| B.氯气具有刺激性气味,可以熏死细菌、病毒 |
| C.氯气与水反应生成具有强氧化性的HClO,可以杀死细菌、病毒 |
| D.氯气用于自来水消毒的工艺简单、成熟,易于操作,且成本低 |