下列相关反应的离子方程式书写错误的是
| A.在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO—+4OH—+2Fe(OH)3=3Cl—+5H2O+2FeO42— |
| B.少量SO2通入苯酚钠溶液中:2C6H5O—+SO2+H2O=2C6H5OH+SO32— |
| C.用稀硫酸酸化的KMnO4溶液与H2O2反应:2MnO4—+6H++5H2O2=2Mn2++5O2↑+8H2O |
| D.少量SO2通入NaClO溶液中:SO2+ClO—+OH—=SO42—+Cl—+H+ |
为了制取碘,可通过反应:2NO+O2==2NO2NO2+2H+ +2I- ="=NO" + I2+H2O制得,NO在制碘过程中的作用是
| A.还原剂 | B.氧化剂 | C.催化剂 | D.反应物 |
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量的关系如图所示。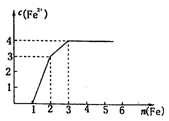
溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为
| A.1:1:1 | B.1:3:1 | C.1:1:4 | D.3:3:8 |
在某100mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.30mol·L-1和0.15mol·L-1。向该混合液中加入3.20g铜粉,加热,待充分反应后,所得溶液中的Cu2+的物质的量浓度(mol·L-1)是
| A.0.225 | B.0.25 | C.0.45 | D.0.50 |
工业废气中氮氧化物是主要的大气污染源之一。
已知:2NO2+2NaOH = NaNO3+NaNO2+H2O,NO2+NO+2NaOH = 2NaNO2+H2O。现有a mol NO2和bmol NO的混合气,若用足量的NaOH溶液将其完全吸收,则混合气中两种气体的物质的量必须满足的关系是:
| A.a=b/3 | B.2a=b | C.a≥b | D.a<b |