在恒压容器a和恒容容器b中,分别充入体积比为1∶3的N2和H2。若开始时两容器的体积相等,且在相同的条件下达到平衡时,两容器的N2的转化率应当是( )
| A.a中大 | B.b中大 | C.a、b一样大 | D.无法判断 |
如图是另一种元素周期表——三角形元素周期表的一部分,图中标出了L、M、Q、R、T元素的位置,下列判断正确的是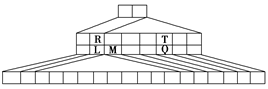
| A.Q、T两元素的简单氢化物的稳定性:HnT<HnQ |
| B.L、R的单质与盐酸反应速率:R>L |
| C.M与T形成的化合物有两性 |
| D.L、Q各自形成的简单离子核外电子数相等 |
下列有关电化学原理的说法中,错误的是
| A.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 |
| B.在铜的精炼装置中,通常用粗铜作作阴极,精铜作阳极 |
| C.氯碱工业,主要依托电解熔融的氯化钠来制取工业上重要的化工原料烧碱和氯气 |
| D.可充电的电池称“二次电池”,在充电时,是将电能转变成化学能,在放电时,又将化学能转化成电能. |
A、B、C三种元素的核电荷数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是
A.a>b>c B.a>c>b C.a=b+m+n D.a=c+n+m
下列各组给定原子序数的元素,不能形成原子数之比为1∶1稳定共价化合物的是
| A.3和17 | B.1和8 | C.6和8 | D.1和6 |
向某一固定体积的密闭容器中充入NO2,在一定条件下进行反应:2NO2 2NO+O2。达到平衡状态的标志是①体系的颜色不再发生变化 ②容器内压强不随时间变化而变化 ③NO和O2的消耗速率之比为2:1 ④容器中c(NO2):c(NO):c(O2)=2:2:1
2NO+O2。达到平衡状态的标志是①体系的颜色不再发生变化 ②容器内压强不随时间变化而变化 ③NO和O2的消耗速率之比为2:1 ④容器中c(NO2):c(NO):c(O2)=2:2:1
| A.①② | B.③④ | C.①④ | D.②③ |