下列有关电化学原理的说法中,错误的是
| A.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 |
| B.在铜的精炼装置中,通常用粗铜作作阴极,精铜作阳极 |
| C.氯碱工业,主要依托电解熔融的氯化钠来制取工业上重要的化工原料烧碱和氯气 |
| D.可充电的电池称“二次电池”,在充电时,是将电能转变成化学能,在放电时,又将化学能转化成电能. |
某强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32―、SO32―、SO42―、C1―、NO2-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下: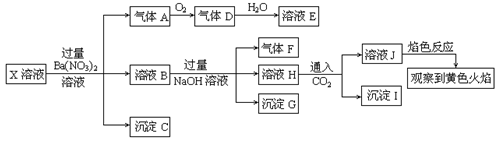
下列结论正确的是
| A.X中肯定存在Na+、Fe2+、A13+、NH4+、SO42― |
| B.气体F经催化氧化可直接生成气体D |
| C.沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3 、沉淀I一定是Al(OH )3 |
| D.X中不能确定的离子是 A13+、Na+、K+和C1― |
下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.在常温常压下,11.2 L N2含有的分子数为0.5 NA |
| B.在常温常压下,1mol Ne含有的原子数为NA |
| C.22.4lCl2所含原子数为2NA |
| D.在同温同压下,相同体积的任何气体单质所含的原子数相同,而Ne由一个原子构成。相同状况下,相同体积的上述气体所含原子数就不相同。 |
设NA为阿伏伽德罗常数的值,下列说法中正确的是
| A.常温下,16gO2和O3的混合气体中含有l.5NA个氧原子 |
| B.常温下,1Llmol·L-1Na2CO3溶液中所含的CO32-为NA |
| C.58g乙烯和乙烷的混合气体中碳原子数目一定为4NA |
| D.常温常压下,足量的Fe在lmolCl2中充分燃烧,转移的电子数为2NA |
短周期元素X的原子最外电子层中具有最多的未成对电子,元素Y的价电子排布式为nsnnpn+2,则X、Y组成的微粒中,不可能存在的是
| A.X2Y5 | B.XY42- | C.XY2- | D.XY3- |
溴、碘主要存在于海水中,有“海洋元素”的美称.海水中的碘富集在海藻中,我国海带产量居世界第一,除供食用外,大量用于制碘.提取碘的途径如下所示:
下列有关叙述正确的是
| A.碘元素在海水中也有游离态存在 |
| B.操作A是结晶或重结晶 |
| C.B是提纯操作,常用蒸馏 |
| D.在提取的过程中用的氧化剂可以是H2O2 |