把0.05 mol NaOH固体分别加入到100 mL下列液体中,溶液的导电能力变化最小的是
| A.自来水 | B.0.5 mol·L-1的盐酸 |
| C.0.5 mol·L-1的CH3COOH溶液 | D.0.5 mol·L-1的KCl溶液 |
已知在25 ℃、101 kPa下,1 g C8H18(l)燃烧生成CO2和液态H2O时放出48.40 kJ的热量,表示上述反应的热化学方程式正确的是
A.C8H18(l)+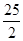 O2(g)===8CO2(g)+9H2O(g)ΔH=-48.40 kJ·mol-1 O2(g)===8CO2(g)+9H2O(g)ΔH=-48.40 kJ·mol-1 |
B.C8H18(l)+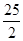 O2(g)===8CO2(g)+9H2O(l)ΔH=-5 517.6 kJ·mol-1 O2(g)===8CO2(g)+9H2O(l)ΔH=-5 517.6 kJ·mol-1 |
C.C8H18(l)+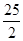 O2(g)===8CO2(g)+9H2O(g) ΔH=+5 517.6 kJ·mol-1 O2(g)===8CO2(g)+9H2O(g) ΔH=+5 517.6 kJ·mol-1 |
| D.2C8H18(l)+25O2(g)===16CO2(g)+18 H2O(l)ΔH=-5 517.6 kJ·mol-1 |
下图是恒温下某反应的化学反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是
| A.反应达平衡时,正反应速率和逆反应速率相等 |
| B.该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ |
| C.该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ |
| D.同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等 |
已知反应4CO+2NO2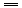 N2+4CO2在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
N2+4CO2在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
| A.v(CO)=1.5 mol·L-1·min-1 | B.v(NO2)=0.7 mol·L-1·min-1 |
| C.v(N2)=0.4 mol·L-1·min-1 | D.v(CO2)=1.1 mol·L-1·min-1 |
100mL 4mol/L 稀硫酸与2g锌粒反应,在一定温度下为了减缓反应的速率,但又不影响生成氢气的总量,可向反应物中加入
| A.硫酸钠固体 | B.硫酸铜固体 | C.硝酸钾溶液 | D.氯化钠溶液 |
下列关于原电池的叙述正确的是
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.原电池是将化学能转变为电能的装置 |
| C.在原电池中,电子流出的一极是负极,该电极被还原 |
| D.原电池放电时,电流的方向是从负极到正极 |